2022.12.22
- プレスリリース
- 研究
COVID-19が重症化する背景メカニズムを解明
発症後早期の肺胞上皮細胞死が引き金となっている可能性
横浜市立大学大学院医学研究科 麻酔科学の東條 健太郎講師らの研究グループは、同研究科 救急医学との共同研究で、新型コロナウイルス感染症(COVID-19)の重症例では、発症後早期に自己の肺組織を構成する上皮細胞の細胞死が生じ、死細胞から放出される分子が重症化の引き金となっている可能性があることを明らかにしました。
本研究成果は、ウイルスそのものだけではなく、細胞死に陥った自己細胞から放出される分子がCOVID-19重症化を予防するための治療標的であることを示しており、新規治療薬の開発への足がかりを与えるものです。
本研究成果は、Cell Pressが刊行する国際学術誌「iScience」に掲載されました。(2022年12月5日オンライン)
本研究成果は、ウイルスそのものだけではなく、細胞死に陥った自己細胞から放出される分子がCOVID-19重症化を予防するための治療標的であることを示しており、新規治療薬の開発への足がかりを与えるものです。
本研究成果は、Cell Pressが刊行する国際学術誌「iScience」に掲載されました。(2022年12月5日オンライン)
研究成果のポイント
|
研究背景
COVID-19では、体内のウイルス量がピークを過ぎた後のタイミングで、病態の重症化が進行することが知られています。しかしながら、ウイルス量が減った後にどのようなメカニズムで、肺組織傷害が進行するのかは分かっていませんでした。
本研究グループは、今までに、急性呼吸促迫症候群(Acute Respiratory Distress Syndrome: ARDS)*3と呼ばれる重症呼吸不全に陥ったCOVID-19症例では、発症後早期に肺組織を構成する肺胞上皮細胞の強い傷害が見られることを明らかにしていました(文献1)。これを踏まえ、初期に生じた肺胞上皮細胞の傷害が、COVID-19の病態を重症化させる引き金になっている可能性があると考え、本研究を行いました。
本研究グループは、今までに、急性呼吸促迫症候群(Acute Respiratory Distress Syndrome: ARDS)*3と呼ばれる重症呼吸不全に陥ったCOVID-19症例では、発症後早期に肺組織を構成する肺胞上皮細胞の強い傷害が見られることを明らかにしていました(文献1)。これを踏まえ、初期に生じた肺胞上皮細胞の傷害が、COVID-19の病態を重症化させる引き金になっている可能性があると考え、本研究を行いました。
研究内容
本研究では最初に、横浜市立大学附属病院に入院した重症COVID-19症例における肺胞上皮細胞の細胞死メカニズムについて、検討を行いました。細胞死は、細胞内のダメージ関連分子パターン(DAMPs)分子を放出し、炎症を引き起こす「ネクローシス」と呼ばれる細胞死と、炎症をほとんど引き起こさない「アポトーシス」と呼ばれる細胞死の2つに分けることができます。血液中および気管支肺胞洗浄液中の特異的マーカーを分析した結果、COVID-19によるARDS患者では、発症早期に主にネクローシスによって上皮細胞死が引き起こされていることが明らかになりました(図1上)。また、同時にCOVID-19によるARDS患者の血液中では、ネクローシス細胞から放出される代表的なDAMPsであるHMGB-1分子の濃度が増加していることが明らかになりました。
次に、COVID-19の原因ウイルスSARS-CoV-2の構成成分をマウスの肺の中に注入することで、COVID-19の動物モデルを作成し、肺胞上皮細胞の細胞死メカニズムを詳しく解析しました。その結果、COVID-19動物モデルでは、ネクロトーシス及びパイロトーシスと呼ばれる、分子的に制御されたネクローシスが生じていることが明らかになりました。さらに、このCOVID-19動物モデルに対して、抗HMGB-1中和抗体を投与することによって、肺組織傷害を軽減できることを確認しました(図1下)。
以上の結果から、COVID-19によるARDSでは、ウイルスそのものだけではなく、発症後早期にネクローシスに陥った肺胞上皮細胞からDAMPsが放出されることで重症化が進行することが示唆されました。
次に、COVID-19の原因ウイルスSARS-CoV-2の構成成分をマウスの肺の中に注入することで、COVID-19の動物モデルを作成し、肺胞上皮細胞の細胞死メカニズムを詳しく解析しました。その結果、COVID-19動物モデルでは、ネクロトーシス及びパイロトーシスと呼ばれる、分子的に制御されたネクローシスが生じていることが明らかになりました。さらに、このCOVID-19動物モデルに対して、抗HMGB-1中和抗体を投与することによって、肺組織傷害を軽減できることを確認しました(図1下)。
以上の結果から、COVID-19によるARDSでは、ウイルスそのものだけではなく、発症後早期にネクローシスに陥った肺胞上皮細胞からDAMPsが放出されることで重症化が進行することが示唆されました。
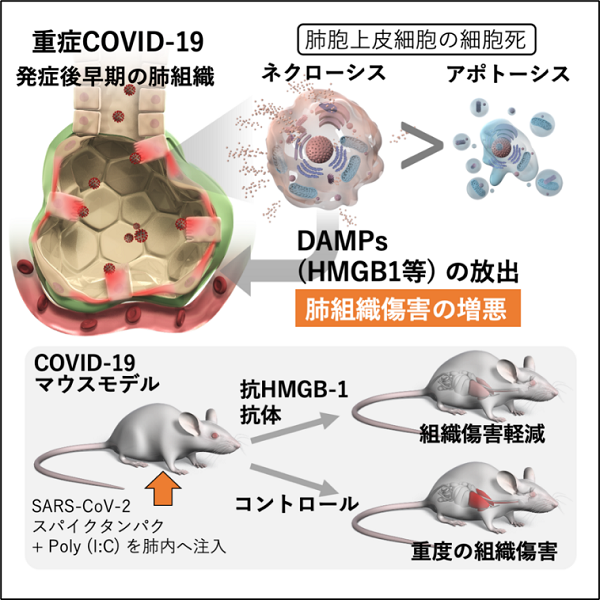
図1 研究概要
上:COVID-19によるARDSにおいて発症後早期に肺胞上皮がネクローシスに陥ることで、組織傷害を増悪させるダメージ関連分子パターン(DAMPs)が放出される。
下:代表的なDAMPsの一つであるHMGB-1分子に対する中和抗体がCOVID-19動物モデルの肺組織傷害を軽減した。
上:COVID-19によるARDSにおいて発症後早期に肺胞上皮がネクローシスに陥ることで、組織傷害を増悪させるダメージ関連分子パターン(DAMPs)が放出される。
下:代表的なDAMPsの一つであるHMGB-1分子に対する中和抗体がCOVID-19動物モデルの肺組織傷害を軽減した。
今後の展開
本研究成果によって、細胞死を引き起こした自己の細胞から放出されるDAMPsが、COVID-19の重症化を防ぐための、有効な治療標的である可能性が示されました。肺胞上皮細胞の細胞死そのものは発症後早期に生じることから、予防的な介入を行うことは難しいと考えられます。しかし、その後放出されるDAMPsを標的とすることで、病院を受診した後であっても重症化を防ぐことができる可能性があり、今後の治療薬開発につながることが期待されます。
研究費
本研究は、日本医療研究開発機構(AMED)、横浜総合医学振興財団、日本学術振興会・科学研究費補助金(科研費)、及び横浜市立大学学術的研究推進事業(学長裁量事業) の支援を受けて実施されました。
論文情報
タイトル: Early alveolar epithelial cell necrosis is a potential driver of COVID-19-induced acute respiratory distress syndrome
著者: Kentaro Tojo, Natsuhiro Yamamoto, Nao Tamada, Takahiro Mihara, Miyo Abe, Mototsugu Nishii, Ichiro Takeuchi, Takahisa Goto
掲載雑誌: iScience
DOI:https://doi.org/10.1016/j.isci.2022.105748
著者: Kentaro Tojo, Natsuhiro Yamamoto, Nao Tamada, Takahiro Mihara, Miyo Abe, Mototsugu Nishii, Ichiro Takeuchi, Takahisa Goto
掲載雑誌: iScience
DOI:https://doi.org/10.1016/j.isci.2022.105748
用語説明
*1 ネクローシス:
細胞死機構の一つ。細胞膜が破綻することで、ダメージ関連分子パターンを含む細胞内容物が周囲に放出され、炎症を引き起こす。過去には、細胞に対する機械的な損傷等によって専ら受動的に生じると考えられていたが、近年、ネクロトーシスやパイロトーシスといった分子的に制御されたタイプのネクローシスの存在が明らかになっている。
*2 ダメージ関連分子パターン(DAMPs):
傷害を受けた自己組織から放出され、パターン認識受容体を介して炎症を引き起こす様々な分子群。HMGB-1は代表的なDAMPsの一つとして知られている。
*3 急性呼吸促迫症候群(ARDS):
肺胞を構成する組織が傷害を受けることにより、肺胞の透過性が亢進することで引き起こされる重症呼吸不全。
細胞死機構の一つ。細胞膜が破綻することで、ダメージ関連分子パターンを含む細胞内容物が周囲に放出され、炎症を引き起こす。過去には、細胞に対する機械的な損傷等によって専ら受動的に生じると考えられていたが、近年、ネクロトーシスやパイロトーシスといった分子的に制御されたタイプのネクローシスの存在が明らかになっている。
*2 ダメージ関連分子パターン(DAMPs):
傷害を受けた自己組織から放出され、パターン認識受容体を介して炎症を引き起こす様々な分子群。HMGB-1は代表的なDAMPsの一つとして知られている。
*3 急性呼吸促迫症候群(ARDS):
肺胞を構成する組織が傷害を受けることにより、肺胞の透過性が亢進することで引き起こされる重症呼吸不全。
参考文献
(文献1)Tojo K, Yamamoto N, Mihara T, Abe M, Goto T. Distinct temporal characteristics of circulating alveolar epithelial and endothelial injury markers in ARDS with COVID-19. Crit Care. 2021 May 17;25(1):169. doi: 10.1186/s13054-021-03596-4.


