2009.05.01
- プレスリリース
- 研究
-全く新しい原理に基づく制癌剤の開発を目指す-
☆研究成果のポイント
○遺伝子変異の蓄積を特徴とするがん細胞の増殖などに関わる「mRNAの品質監視のスイッチ 機構」の解明に成功
→全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法の開発などに、大きな弾みをつける成果
→全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法の開発などに、大きな弾みをつける成果
横浜市立大学大学院医学研究科分子細胞生物学・山下暁朗客員准教授(独立行政法人科学技術振興機構さきがけ研究者)、同大学院博士課程4年生・泉奈津子氏らによる先端医科学研究センターの研究グループが、ナンセンスmRNAを検出する分子複合体を同定し、mRNAの品質監視の分子機構の解明に成功しました。
これは、全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法の開発などに大きな弾みをつける成果です。本研究は、先端医科学研究センター・大野茂男教授、平野久教授らが推進している研究開発プロジェクトの成果の一つでもあります。
これは、全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法の開発などに大きな弾みをつける成果です。本研究は、先端医科学研究センター・大野茂男教授、平野久教授らが推進している研究開発プロジェクトの成果の一つでもあります。
☆研究の背景
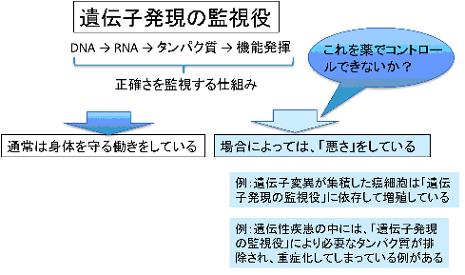
ゲノムDNAにコードされた遺伝情報は、RNAを通じてタンパク質に翻訳されます。最近の研究から、異常なタンパク質を作らせないための仕組みとして、DNAからタンパク質への一連の過程を監視する「遺伝子発現の監視役」があることが明らかとなりつつあります。
本研究グループは、「遺伝子発現の監視役」の一つである「ナンセンスmRNA分解」に着目し、SMG-1というタンパク質リン酸化酵素がその要であることを示してきました。しかしそのスイッチのオンオフの仕組みは謎でした。一方、本研究グループは、通常身体を守っている免疫系が時として「悪さ」をするように、本来身体を守るべき「遺伝子発現の監視役」が、場合によっては「悪さ」をしていることも示してきました。例えば、遺伝子変異の蓄積を特徴とするがん細胞の増殖は、「遺伝子発現の監視役」に大きく依存しています。また、遺伝子変異に起因する遺伝性疾患においては、排除される必要のないRNAが排除されてしまっている例があります。つまり、免疫抑制剤と同様に、この仕組みの抑制が役に立つ場合があることが期待できます。
本研究グループは、「遺伝子発現の監視役」の一つである「ナンセンスmRNA分解」に着目し、SMG-1というタンパク質リン酸化酵素がその要であることを示してきました。しかしそのスイッチのオンオフの仕組みは謎でした。一方、本研究グループは、通常身体を守っている免疫系が時として「悪さ」をするように、本来身体を守るべき「遺伝子発現の監視役」が、場合によっては「悪さ」をしていることも示してきました。例えば、遺伝子変異の蓄積を特徴とするがん細胞の増殖は、「遺伝子発現の監視役」に大きく依存しています。また、遺伝子変異に起因する遺伝性疾患においては、排除される必要のないRNAが排除されてしまっている例があります。つまり、免疫抑制剤と同様に、この仕組みの抑制が役に立つ場合があることが期待できます。
☆ 研究の概要
本研究グループは、今回、タンパク質リン酸化酵素であるSMG-1が新規のサブユニットと協調して「ナンセンスmRNA分解」の引き金を引くことを見いだしました。同時に、ナンセンスmRNAを検出している分子複合体の同定、分離に成功しました。また、今回の発見が多細胞生物の種を超えて進化的に保存されている基本的な仕組みであることも見いだしました。
まず、新規SMG-1サブユニットの一つであるSMG-8が通常SMG-1の活性を抑制していることを見つけました。さらに、異常なmRNAを認識する分子複合体の形成過程では、SMG-1の活性化を担っていることも突き止めました。つまり、SMG-8はSMG-1の「活性の抑制」の役割と同時に、「活性化」という二つの役割を担っています。SMG-8がSMG-1の活性を調節している要であることがわかったことになります。
今回のSMG-1の活性のスイッチのオンとオフの機構の解明とナンセンスmRNAを検出している分子複合体の同定は、全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法、診断法の開発などに、大きな弾みをつける成果です。
まず、新規SMG-1サブユニットの一つであるSMG-8が通常SMG-1の活性を抑制していることを見つけました。さらに、異常なmRNAを認識する分子複合体の形成過程では、SMG-1の活性化を担っていることも突き止めました。つまり、SMG-8はSMG-1の「活性の抑制」の役割と同時に、「活性化」という二つの役割を担っています。SMG-8がSMG-1の活性を調節している要であることがわかったことになります。
今回のSMG-1の活性のスイッチのオンとオフの機構の解明とナンセンスmRNAを検出している分子複合体の同定は、全く新しい原理に基づく制がん剤の開発や、重症の遺伝性疾患に対する遺伝子変異に応じた治療法、診断法の開発などに、大きな弾みをつける成果です。
☆ナンセンスmRNAとは
がんや遺伝性疾患などにおける遺伝子変異の約1/3がナンセンスmRNAと呼ばれる異常なmRNAを生じるタイプの変異であると言われています。ナンセンスmRNAは末端が欠落した異常タンパク質の合成を指令します。細胞は、この異常タンパク質の毒性に対する防御機構として、ナンセンスmRNAを認識して、分解排除する遺伝子発現の品質監視機構を備えています。この品質監視機構は、遺伝子の異常に由来するがんや遺伝性疾患などの症状に大きな影響を与えます。
※ 本研究成果は米国の分子生物学専門誌『Genes & Development』5月1日号に掲載されます。
Yamashita A, Izumi N, Kashima I, Ohnishi T, Saari B, Katsuhata Y, Muramatsu R, Morita T, Iwamatsu A, Hachiya T, Kurata R, Hirano H, Anderson P, and Ohno S.
SMG-8 and SMG-9, two novel subunits of the SMG-1 complex, regulate remodeling of the mRNA surveillance complex during nonsense-mediated mRNA decay.
Genes & Development, 23 (9), 2009.
※ 本研究は、文部科学省科学研究費、独立行政法人科学技術振興機構さきがけ研究などの助成により行われました。
Yamashita A, Izumi N, Kashima I, Ohnishi T, Saari B, Katsuhata Y, Muramatsu R, Morita T, Iwamatsu A, Hachiya T, Kurata R, Hirano H, Anderson P, and Ohno S.
SMG-8 and SMG-9, two novel subunits of the SMG-1 complex, regulate remodeling of the mRNA surveillance complex during nonsense-mediated mRNA decay.
Genes & Development, 23 (9), 2009.
※ 本研究は、文部科学省科学研究費、独立行政法人科学技術振興機構さきがけ研究などの助成により行われました。