マウス多能性幹細胞から精巣組織の再構築に成功
-機能的な体細胞を誘導し、精子形成不全の回復と産子獲得を実証-
横浜市立大学大学院医学研究科 臓器再生医学教室の佐藤卓也講師、小川毅彦特別教授、大阪大学ヒューマン・メタバース疾患研究拠点(WPI-PRIMe)の吉野剛史特任准教授(常勤)、同大学院医学系研究科ゲノム生物学(生殖遺伝学)の林克彦教授(ヒューマン・メタバース疾患研究拠点副拠点長)、理化学研究所生命医科学研究センターの鈴木貴紘客員主管研究員、同バイオリソース研究センターの小倉淳郎副センター長らの研究グループは、東京大学、久留米大学との共同研究により、マウス多能性幹細胞*1から機能的な精巣体細胞*2を誘導し、精子形成を支える精巣組織を試験管内で再構築して、産子獲得に成功しました。本技術は、男性不妊の治療法開発だけでなく、化学物質等が及ぼす生殖毒性を評価する動物実験代替法としての活用も期待され、創薬や化学工業分野の発展にも貢献します。
本研究成果は、米国科学振興協会(AAAS)が発行するオンライン学術雑誌「Science Advances」に掲載されました(米国東部時間2026年2月26日14時)。
同日付けの米国科学誌「Science」には、本研究と並行して横浜市立大学と共同研究を実施してきた、大阪大学主導の関連研究の成果(多能性幹細胞から精巣を試験管内で作り出し、精子産生能を持つ精原幹細胞の誘導に成功)が掲載されました。
本研究成果は、米国科学振興協会(AAAS)が発行するオンライン学術雑誌「Science Advances」に掲載されました(米国東部時間2026年2月26日14時)。
同日付けの米国科学誌「Science」には、本研究と並行して横浜市立大学と共同研究を実施してきた、大阪大学主導の関連研究の成果(多能性幹細胞から精巣を試験管内で作り出し、精子産生能を持つ精原幹細胞の誘導に成功)が掲載されました。
本研究成果のポイント
● マウス多能性幹細胞から、精子形成を支える精巣組織の再構築に成功
● 再構築した組織を用いることで精子形成不全を改善し、顕微授精により健常な産子獲得を実証
● 男性不妊の治療研究や、化学物質の生殖毒性を調べる動物実験代替法への応用に期待
研究背景
本研究グループの佐藤らは、2011年に、マウスの精巣組織を体外で培養し、精子幹細胞から精子産生に至る全過程を再現することに成功しました[参考文献1]。この体外精子形成法は、精子形成メカニズムの解明や、化学物質の毒性試験などの動物実験代替法として期待されています。しかし、従来の培養方法では、マウス個体から採取した生体の精巣組織を培養に用いるため、実験のたびに動物からの組織提供が不可欠であるという制限がありました。そこで本研究では、この課題を克服するため、生体材料に依存することなく、多能性幹細胞(ES細胞)から精子形成を支える精巣体細胞そのものを人工的に作製し、試験管内で精子形成環境を構築する技術の確立を目指しました。
研究内容
本研究グループは、これまでに報告されていた多能性幹細胞から卵巣体細胞を分化誘導する手法(Yoshino et al., Science 2021[参考文献2])を基盤に、発生学的な知見に基づいた改良を加えることで、精巣体細胞への分化を促す新たな培養法を確立しました。具体的には、ES細胞から精巣が形成されるまでの段階的な発生過程を試験管内で再現する誘導工程において、最終段階で、卵巣への分化を促す働きを持つWntシグナルを阻害する化合物(IWR1)を添加する手法を開発しました。このシグナル制御により、卵巣への分化を抑え、精巣分化に不可欠な転写因子であるNr5a1やGata4を発現する胎仔(たいじ)期精巣体様細胞(fTeSLCs)を効率的に作製することに成功しました。さらに、次世代シーケンサーを用いた1細胞ごとの網羅的遺伝子発現解析(scRNA-seq解析)を行った結果、誘導された細胞群は、生体の胎仔精巣と同様に、セルトリ細胞やライディッヒ細胞の前駆細胞などに相当する多様な細胞種を含んでいることが確認されました。
この細胞群を用いて、以下の通り機能を実証しました(図1)。
2. 機能の証明:再構築された精巣組織内において、誘導されたセルトリ細胞によって精細管構造が形成され、その内部で停止していた精子形成が再開することを確認しました。また、別の疾患モデルを用いた検証により、移植した前駆細胞が機能的なライディッヒ細胞へと分化し、精子形成を支持する能力を持つことを実証しました。その結果、いずれの系においても減数分裂を経て精子細胞まで分化することが確認されました。
3. 産子獲得:得られた精子細胞を用いて顕微授精(ROSI)を行ったところ、健康な産子が誕生し、正常に成育して次世代を残せることを世界で初めて実証しました。
この細胞群を用いて、以下の通り機能を実証しました(図1)。
1. 精巣組織の再構築: 誘導した細胞(セルトリ細胞様細胞およびライディッヒ細胞の前駆細胞を含む細胞群)を、特定の体細胞が欠損して精子を作ることができない疾患モデルマウスの精巣内にそれぞれ移植しました。その結果、移植された細胞は精巣内の適切な場所に定着し、精子形成の場となる精細管の構造や、その周囲の間質といった精巣特有の複雑な組織構造を再構築することを確認しました。
2. 機能の証明:再構築された精巣組織内において、誘導されたセルトリ細胞によって精細管構造が形成され、その内部で停止していた精子形成が再開することを確認しました。また、別の疾患モデルを用いた検証により、移植した前駆細胞が機能的なライディッヒ細胞へと分化し、精子形成を支持する能力を持つことを実証しました。その結果、いずれの系においても減数分裂を経て精子細胞まで分化することが確認されました。
3. 産子獲得:得られた精子細胞を用いて顕微授精(ROSI)を行ったところ、健康な産子が誕生し、正常に成育して次世代を残せることを世界で初めて実証しました。
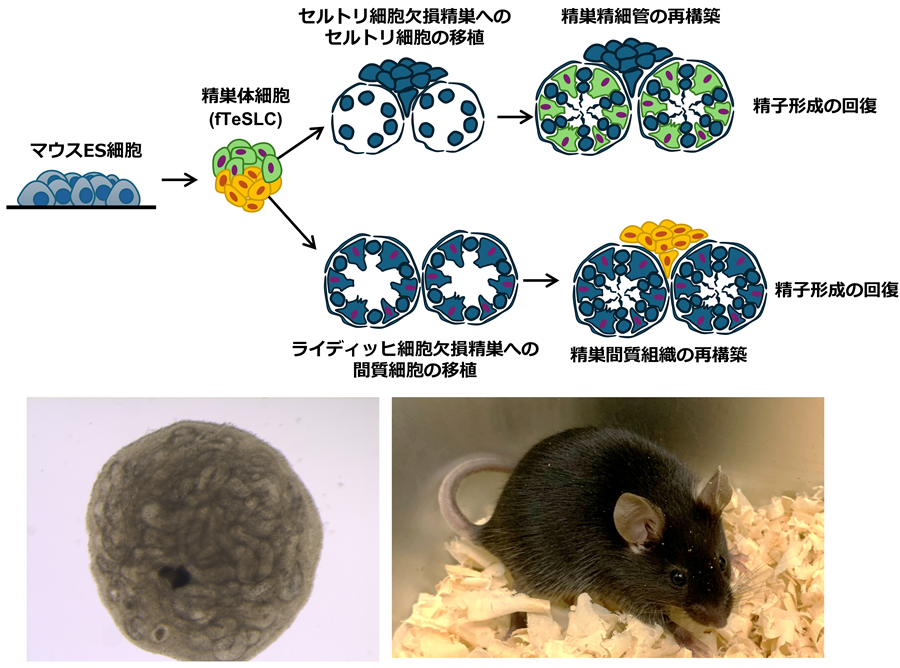

マウス多能性幹細胞(ES細胞)から、精巣を構成する主要な体細胞(セルトリ細胞・ライディッヒ前駆細胞)を誘導。これを体細胞欠損モデルマウスへ移植することで、精子形成を支える組織構造(精細管*3(左下写真)・間質*4)の再構築に成功した。その結果、停止していた精子形成が再開し、得られた精子細胞を用いた顕微授精により、健康な産子を獲得した(右下写真)。
今後の展開
本研究成果は、精子形成を支える環境を人工的に作り出せることを示しました。これにより、以下のような医学・産業の両面で大きな波及効果が期待されます。
• 男性不妊治療への応用: 精巣の組織や機能に問題がある造精機能障害などの男性不妊に対し、将来的にiPS細胞等から再構築した精巣組織を活用して治療する新たな医療開発につながることが期待されます。
• 動物実験代替法への活用: 薬剤が精子形成に与える影響(生殖毒性)を、試験管内で再構築した精巣組織を用いて評価するシステムの開発が可能です。これにより、実験動物の使用を減らすとともに、より効率的な創薬や安全性評価への貢献が期待されます。
• 性決定および精巣形成メカニズムの解明: 未だ多くの謎に包まれている性決定や精巣形成の基礎的な分子メカニズムを解明するための、強力な解析ツールとなります。
• 男性不妊治療への応用: 精巣の組織や機能に問題がある造精機能障害などの男性不妊に対し、将来的にiPS細胞等から再構築した精巣組織を活用して治療する新たな医療開発につながることが期待されます。
• 動物実験代替法への活用: 薬剤が精子形成に与える影響(生殖毒性)を、試験管内で再構築した精巣組織を用いて評価するシステムの開発が可能です。これにより、実験動物の使用を減らすとともに、より効率的な創薬や安全性評価への貢献が期待されます。
• 性決定および精巣形成メカニズムの解明: 未だ多くの謎に包まれている性決定や精巣形成の基礎的な分子メカニズムを解明するための、強力な解析ツールとなります。
用語説明
*1 多能性幹細胞:胚性幹細胞(ES細胞)や人工多能性幹細胞(iPS細胞)のように、体中のほぼすべての種類の細胞に分化する能力(多能性)と、無限に増殖する能力を併せ持つ細胞のこと。
*2 精巣体細胞:精巣を構成する細胞のうち、精子のもとになる「生殖細胞」以外の細胞。代表的なものに、生殖細胞を直接サポートするセルトリ細胞や、男性ホルモン(アンドロゲン)を産生するライディッヒ細胞がある。これらは精子形成が正常に進行するために不可欠な環境を形作っている。
*3 精細管:精巣内にある細い管状の構造。内部に生殖細胞とセルトリ細胞を収めており、精子形成が行われる直接の「場」となる。
*4 間質:精巣内において、精細管の間を埋めている組織。ここにはライディッヒ細胞や血管などが存在し、男性ホルモンの供給や微小環境の維持を担っている。
*2 精巣体細胞:精巣を構成する細胞のうち、精子のもとになる「生殖細胞」以外の細胞。代表的なものに、生殖細胞を直接サポートするセルトリ細胞や、男性ホルモン(アンドロゲン)を産生するライディッヒ細胞がある。これらは精子形成が正常に進行するために不可欠な環境を形作っている。
*3 精細管:精巣内にある細い管状の構造。内部に生殖細胞とセルトリ細胞を収めており、精子形成が行われる直接の「場」となる。
*4 間質:精巣内において、精細管の間を埋めている組織。ここにはライディッヒ細胞や血管などが存在し、男性ホルモンの供給や微小環境の維持を担っている。
研究費
本研究は、JSPS科研費(18H05546、22H00485、20H03437、20K21657、24K21284、19H05758、19K06678、23K18078、23H04949、23K20043、24H00059、23H04956、20H04926)、AMED(JP24mk0121304)、JST(JPMJFR2451)、JSPS世界トップレベル研究拠点プログラム(WPI)、横浜市立大学学長裁量事業 戦略的研究推進事業(SK2811、SK202403)の支援を受けて実施されました。
論文情報
タイトル:Generation of Functionally Competent Testicular Somatic Cells from Pluripotent Stem Cells
著者:Takuya Sato, Takashi Yoshino, Mai Ohtsuka, Takahiro Suzuki, Takafumi Matsumura, Yuki Matsudaira, Yu Ishikawa-Yamauchi, Shiori Maeda, Haruka Yabukami, Yoshiakira Kanai, Miki Inoue, Yuichi Shima, Makoto Tachibana, Shogo Matoba, Kimiko Inoue, Narumi Ogonuki, Atsuo Ogura, Katsuhiko Hayashi, Takehiko Ogawa
掲載雑誌:Science Advances
DOI:10.1126/sciadv.adz0269
※同日付けの米国科学誌「Science」には、本研究と並行して横浜市立大学と共同研究を実施してきた、大阪大学主導の関連研究の成果が掲載されます(DOI:10.1126/science.aea0296)。詳細は大阪大学発表のプレスリリースをご覧ください。
著者:Takuya Sato, Takashi Yoshino, Mai Ohtsuka, Takahiro Suzuki, Takafumi Matsumura, Yuki Matsudaira, Yu Ishikawa-Yamauchi, Shiori Maeda, Haruka Yabukami, Yoshiakira Kanai, Miki Inoue, Yuichi Shima, Makoto Tachibana, Shogo Matoba, Kimiko Inoue, Narumi Ogonuki, Atsuo Ogura, Katsuhiko Hayashi, Takehiko Ogawa
掲載雑誌:Science Advances
DOI:10.1126/sciadv.adz0269
※同日付けの米国科学誌「Science」には、本研究と並行して横浜市立大学と共同研究を実施してきた、大阪大学主導の関連研究の成果が掲載されます(DOI:10.1126/science.aea0296)。詳細は大阪大学発表のプレスリリースをご覧ください。
お問い合わせ先

