抗ヘルペスウイルス薬が働く仕組みを原子レベルで解明 ~実験と計算を組み合わせ、次世代抗ウイルス薬開発への道を開く~
研究成果のポイント
● ヘルペスウイルスの増殖に必須なタンパク質と薬剤の複合体構造を決定
● 酵素の動きと薬剤の結合強度を計算化学で検証し、薬剤の作用を定量的に解明
● 新たな抗ウイルス薬設計につながる構造情報を提供
研究背景
ヘルペスウイルスは、多くの人が感染する身近なウイルスです。これまでに8種類のヒトヘルペスウイルスが知られており、単純ヘルペスや水痘、帯状疱疹などの感染症を引き起こします。特に免疫力が低下した人では、重篤な病気につながることがあります。また近年では、自己免疫疾患や認知症との関連も報告され、社会的な関心が高まっています。一方で、現在使用されている抗ヘルペスウイルス薬の中には、一部のウイルスにしか効果を示さないものがあり、さらに副作用や耐性ウイルスの出現といった課題も抱えています。そのため、新しい治療法の開発が求められてきました。
ヘルペスウイルスは、自己のDNAを複製するために専用のタンパク質を持っています。その中心的な役割を担うのが、「ヘリケース・プライメース複合体(HPC)」と呼ばれるタンパク質複合体です。近年、単純ヘルペスウイルスや帯状疱疹ウイルスのHPCを標的とする新しいタイプの薬剤が使われ始めています。しかし、HPCの詳しい立体構造や、薬剤がどのようにHPCを阻害するかについては、長らく十分に解明されていませんでした。
ヘルペスウイルスは、自己のDNAを複製するために専用のタンパク質を持っています。その中心的な役割を担うのが、「ヘリケース・プライメース複合体(HPC)」と呼ばれるタンパク質複合体です。近年、単純ヘルペスウイルスや帯状疱疹ウイルスのHPCを標的とする新しいタイプの薬剤が使われ始めています。しかし、HPCの詳しい立体構造や、薬剤がどのようにHPCを阻害するかについては、長らく十分に解明されていませんでした。
研究内容
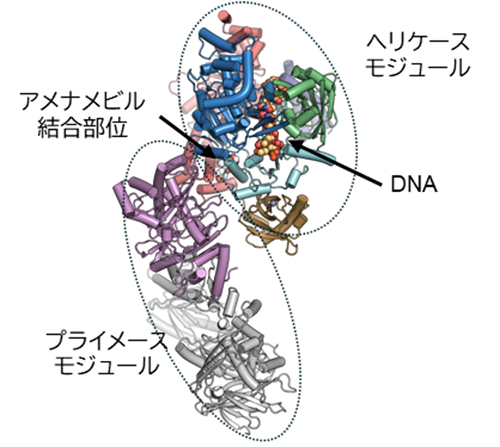
本研究では、クライオ電子顕微鏡*1を用いて、単純ヘルペスウイルス由来のHPCがDNAと、2種類の阻害剤(アメナメビル*2またはプリテリビル*3)のいずれかを結合した状態の立体構造を決定しました(図1)。その結果、HPCは、二本鎖DNAをほどく反応を担うヘリケースモジュールと、RNAプライマーの合成を担うプライメースモジュールからなる構造をとることが明らかになりました。DNAおよび阻害剤はいずれもヘリケースモジュールに結合していました。

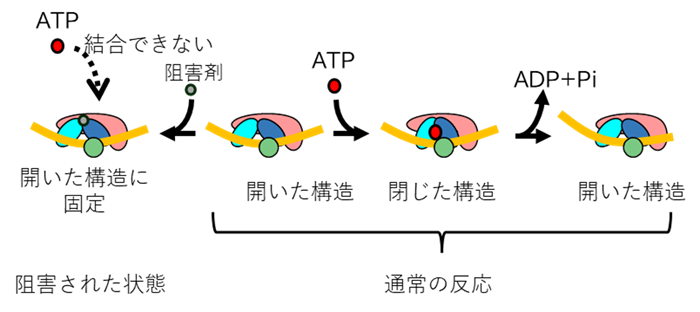
ヘリケース反応では、ATPの結合と加水分解を伴ってタンパク質が立体構造を変化させながら「開いた構造」と「閉じた構造」を繰り返し、尺取り虫のような動きでDNA上を進行します。本研究で得られた阻害剤結合構造は、「開いた構造」に対応していました。さらに、分子動力学シミュレーション*4を行ったところ、阻害剤が結合している場合には、HPCが閉じた構造へと変化しにくくなることが示唆されました。これらの結果から、阻害剤はHPCに結合してその構造を開いた状態に固定し、DNA複製反応を妨げることで抗ウイルス作用を示すと考えられました(図2)。

アメナメビルは単純ヘルペスウイルスおよび帯状疱疹ウイルスに対して効果を示しますが、エプスタイン・バー・ウイルスやサイトメガロウイルスなど、他の臨床的に重要なヘルペスウイルスには効果がありません。一方、プリテリビルは単純ヘルペスウイルスには有効であるものの、帯状疱疹ウイルスを含む他のヘルペスウイルスには弱い効果しか示しません。
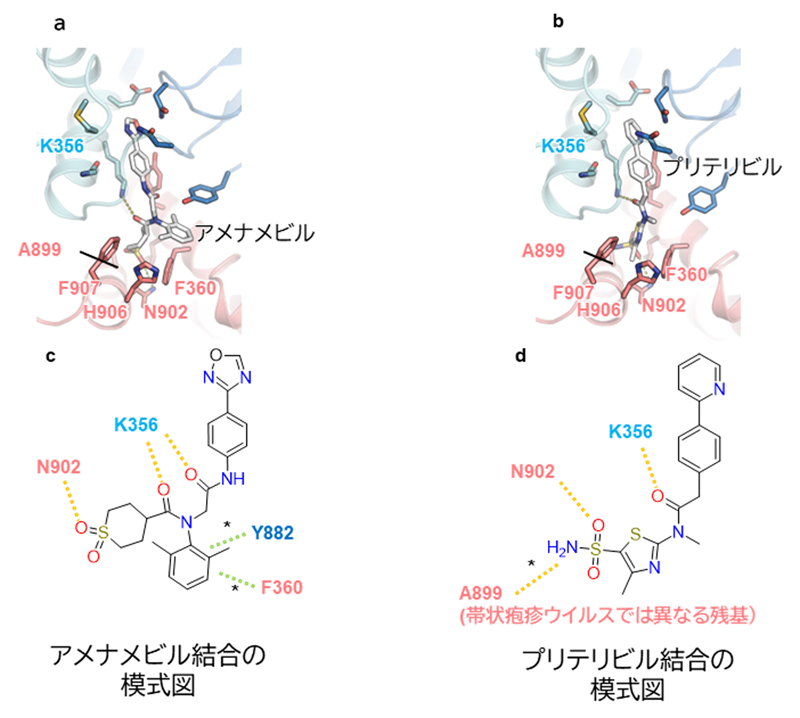
これらのウイルス種による薬効の違いを理解するため、本研究では、量子化学計算法の一種であるフラグメント分子軌道計算*5を分子動力学シミュレーションと組み合わせて用い、薬剤とタンパク質との相互作用を詳細に調べました。その結果、両薬剤の結合に重要なタンパク質残基の一部が、他のヘルペスウイルスでは異なっていることが分かりました(図3a, bのピンク色の残基)。さらに、アメナメビルおよびプリテリビルとタンパク質の間に特徴的な相互作用を見出し(図3c, dの*で示す)、プリテリビルの結合に重要な残基(A899)が帯状疱疹ウイルスでは異なっており、そのために結合が弱められることが示唆されました。これらの結果は、薬剤が一部のヘルペスウイルスに弱い効果しか持たない理由を説明するとともに、それらにも有効な次世代HPC阻害剤の合理的な設計に有用な情報を与えるものです。
これらのウイルス種による薬効の違いを理解するため、本研究では、量子化学計算法の一種であるフラグメント分子軌道計算*5を分子動力学シミュレーションと組み合わせて用い、薬剤とタンパク質との相互作用を詳細に調べました。その結果、両薬剤の結合に重要なタンパク質残基の一部が、他のヘルペスウイルスでは異なっていることが分かりました(図3a, bのピンク色の残基)。さらに、アメナメビルおよびプリテリビルとタンパク質の間に特徴的な相互作用を見出し(図3c, dの*で示す)、プリテリビルの結合に重要な残基(A899)が帯状疱疹ウイルスでは異なっており、そのために結合が弱められることが示唆されました。これらの結果は、薬剤が一部のヘルペスウイルスに弱い効果しか持たない理由を説明するとともに、それらにも有効な次世代HPC阻害剤の合理的な設計に有用な情報を与えるものです。

今後の展開
本研究により、現在使用されているHPC阻害剤がどのように作用してウイルス増殖を抑えるのかについて、原子レベルでの詳細な理解が得られました。これらの知見は、異なるヘルペスウイルスに対しても効果を示す次世代ヘリケース・プライメース複合体阻害剤の開発に向けた重要な基盤情報となります。将来的には、こうした阻害剤が、さまざまなヘルペスウイルス感染症に対する治療薬として、幅広く利用されることが期待されます。
用語説明
*1 クライオ電子顕微鏡:試料を急速に凍結した状態で観察し、タンパク質などの立体構造を高い分解能で解析できる顕微鏡技術。
*2 アメナメビル:ヘルペスウイルスのDNA複製に必須なヘリケース・プライメース複合体を阻害する抗ヘルペスウイルス薬(商品名:アメナリーフ)。日本で単純ヘルペスや帯状疱疹などの治療薬として使われている。
*3 プリテリビル:ヘリケース・プライメース複合体を標的とする抗ヘルペスウイルス薬候補。現在、臨床試験が進められている。
*4 分子動力学シミュレーション:コンピュータ上で分子の動きや構造変化を時間的に再現し、タンパク質の柔軟な挙動を解析する計算手法。
*5 フラグメント分子軌道法(FMO法):タンパク質を小さな部分に分け、それぞれと薬剤との相互作用の強さを量子化学計算により定量的に評価する手法。
*2 アメナメビル:ヘルペスウイルスのDNA複製に必須なヘリケース・プライメース複合体を阻害する抗ヘルペスウイルス薬(商品名:アメナリーフ)。日本で単純ヘルペスや帯状疱疹などの治療薬として使われている。
*3 プリテリビル:ヘリケース・プライメース複合体を標的とする抗ヘルペスウイルス薬候補。現在、臨床試験が進められている。
*4 分子動力学シミュレーション:コンピュータ上で分子の動きや構造変化を時間的に再現し、タンパク質の柔軟な挙動を解析する計算手法。
*5 フラグメント分子軌道法(FMO法):タンパク質を小さな部分に分け、それぞれと薬剤との相互作用の強さを量子化学計算により定量的に評価する手法。
研究費
本研究は、JSPS科研費基盤B(25K02501)、住友財団、シオノギ感染症研究振興財団、上原記念生命科学財団、AMED創薬等先端技術支援基盤プラットフォーム(BINDS)「高難度膜タンパク質等の調製と構造解析可能なグリッド調製の支援」、「ウェットデータとドライデータの統合解析による分子モデリング支援」、「AIとFMO法を融合したインシリコスクリーニングと分子間相互作用解析支援」の支援を受けて実施されました。また、フラグメント分子軌道計算にはスーパーコンピュータ「富岳」(課題番号hp240162)を利用しました。
論文情報
タイトル:Structural insights into inhibition mechanism of the helicase-primase complex from human herpesvirus 1
著者:佐藤光、石田恒、宮岸澄真、小林俊介、木瀬孔明、濱田恵輔、岡田千佳子、小國麻子、濡木理、河野秀俊、福澤薫、仙石徹
掲載雑誌:Cell Chemical Biology
DOI:10.1016/j.chembiol.2026.03.006
著者:佐藤光、石田恒、宮岸澄真、小林俊介、木瀬孔明、濱田恵輔、岡田千佳子、小國麻子、濡木理、河野秀俊、福澤薫、仙石徹
掲載雑誌:Cell Chemical Biology
DOI:10.1016/j.chembiol.2026.03.006
お問合わせ先
横浜市立大学 広報担当
mail: koho@yokohama-cu.ac.jp
mail: koho@yokohama-cu.ac.jp

