特定の周波数の交流磁場が抗腫瘍効果を持つことを発見
—脳腫瘍の画期的な治療機器の開発へ前進—
医工連携・産学連携で日本初の医療機器開発を目指す
横浜市立大学医学部循環制御医学の梅村将就准教授、永迫茜助手らの研究グループは、医学部だけでなく、医工連携や企業との産学連携を通じて、特定の周波数の交流磁場*1が、がん細胞の増殖を抑える働きがあることを発見しました。このユニークな作用は、将来、脳腫瘍をはじめとした新しいがん治療装置の開発に役立つことが期待されます。
本研究成果は、査読付き科学英文誌「Cancer Science」に掲載されました(2024年6月15日)。さらにこの成果は、本誌が選ぶハイライト記事に選出されました。
本研究成果は、査読付き科学英文誌「Cancer Science」に掲載されました(2024年6月15日)。さらにこの成果は、本誌が選ぶハイライト記事に選出されました。
研究成果のポイント
● 特定の周波数の交流磁場が、複数の種類のがん細胞に対して抗腫瘍効果を持つことを見出しました。
● 交流磁場は正常細胞と比較しがん細胞に強く効果を示すことから、副作用が少ない治療法に応用できる可能性があります。
● この発見は、脳腫瘍に対する新しい治療装置の開発に繋がることが期待されます。
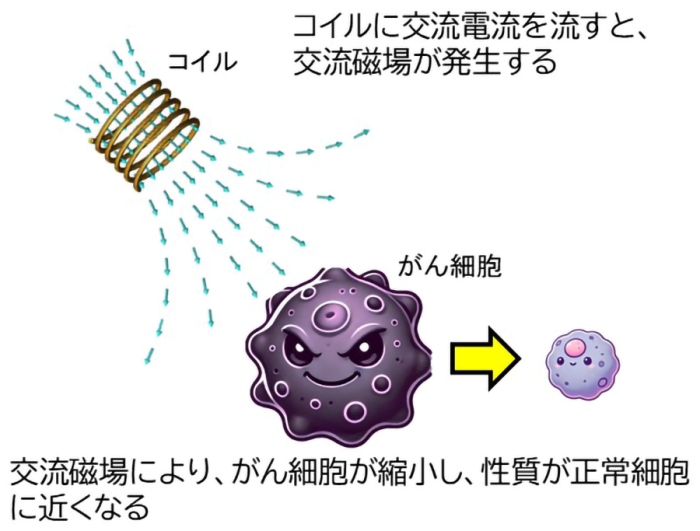

研究背景
悪性神経膠腫*2は、新規患者数が国内で年間3,700 人いるとされ、5年生存率が10%に満たない極めて予後不良な疾患です。初めて診断された場合、標準治療は開頭手術による腫瘍摘出後、放射線治療や薬物療法が行われていますが、治療終了後1年以内に半数以上が再発します。また、再発に至っては標準治療がないため、新しい治療が求められていました。
研究内容
研究グループは悪性神経膠腫や膵がん、乳がん細胞において、特定の周波数の交流磁場が物理刺激のみでがん細胞の増殖を抑える作用(抗腫瘍効果)があることを発見しました。がん細胞では酸素を使わない細胞質でのエネルギー産生方式が一般的ですが、交流磁場の物理的な刺激により、正常細胞のようにミトコンドリア*3で酸素を使うエネルギー産生方式に変わることで、がん細胞の増殖抑制効果を発揮することが本研究で明らかになりました。また、酸素の消費が増えることで活性酸素*4も増え、これががん細胞に作用していると考えられます。
交流磁場刺激により、複数の種類のヒト悪性神経膠腫細胞(脳腫瘍)の増殖が抑制された一方で、正常細胞であるアストロサイト*5には影響しませんでした。また、ヒト悪性神経膠腫細胞を脳に移植したマウスモデルでは、交流磁場の治療(毎日30分/21日間)により、腫瘍の増大を抑制し、全生存期間*6が延長しました。交流磁場の抗腫瘍効果は、ミトコンドリア複合体IVの阻害剤を使ったミトコンドリアの機能停止、または活性酸素除去剤により減少しました。また、交流磁場により、細胞外酸性化速度の減少や酸素消費率の増加が観察されました。これは交流磁場が、がん細胞の代謝から正常細胞へのエネルギー代謝へのシフト(再プログラミング)を誘発することを示唆していると考えられます。以上のことから、交流磁場は物理刺激により、がん細胞の代謝形式を変えることで腫瘍を抑制する、新しい治療戦略になることが期待されます。
交流磁場刺激により、複数の種類のヒト悪性神経膠腫細胞(脳腫瘍)の増殖が抑制された一方で、正常細胞であるアストロサイト*5には影響しませんでした。また、ヒト悪性神経膠腫細胞を脳に移植したマウスモデルでは、交流磁場の治療(毎日30分/21日間)により、腫瘍の増大を抑制し、全生存期間*6が延長しました。交流磁場の抗腫瘍効果は、ミトコンドリア複合体IVの阻害剤を使ったミトコンドリアの機能停止、または活性酸素除去剤により減少しました。また、交流磁場により、細胞外酸性化速度の減少や酸素消費率の増加が観察されました。これは交流磁場が、がん細胞の代謝から正常細胞へのエネルギー代謝へのシフト(再プログラミング)を誘発することを示唆していると考えられます。以上のことから、交流磁場は物理刺激により、がん細胞の代謝形式を変えることで腫瘍を抑制する、新しい治療戦略になることが期待されます。
今後の展開
今後は、このユニークな現象を医療機器開発に応用し、脳腫瘍を始めとしたがん治療ための日本初の画期的な医療装置の作製を目指します。
研究費
本研究は、AMED 医療分野研究成果展開事業(先端計測分析技術・機器開発プログラム)、JST創発的研究支援事業、AMED 令和5-6年度「橋渡し研究プログラム」橋渡し研究支援プログラム(慶應義塾大学拠点)、株式会社リコーの支援を受けて実施されました。
論文情報
タイトル: Alternative magnetic field exposure suppresses tumor growth via metabolic reprogramming
著者: Taisuke Akimoto, Md Rafikul Islam, Akane Nagasako, Kazuhito Kishi,Rina Nakakaji, Makoto Ohtake, Hisashi Hasumi, Takashi Yamaguchi, Shigeki Yamada, Tetsuya Yamamoto, Yoshihiro Ishikawa, Masanari Umemura
掲載雑誌: Cancer Science
DOI: 10.1111/cas.16243
著者: Taisuke Akimoto, Md Rafikul Islam, Akane Nagasako, Kazuhito Kishi,Rina Nakakaji, Makoto Ohtake, Hisashi Hasumi, Takashi Yamaguchi, Shigeki Yamada, Tetsuya Yamamoto, Yoshihiro Ishikawa, Masanari Umemura
掲載雑誌: Cancer Science
DOI: 10.1111/cas.16243
用語解説
*1 交流磁場:電流が一定の方向に流れずに、時間とともに周期的に方向が変わる電流によって発生する磁場のこと。
*2 悪性神経膠腫:脳や脊髄の神経膠細胞から発生する非常に悪性度の高いがん。進行が早く、治療が難しいことが特徴。
*3 ミトコンドリア: 細胞内でエネルギーを生産する「発電所」のような役割を果たす小さな構造体。呼吸によって細胞が必要とするエネルギーを作り出す。
*4 活性酸素:酸素が不安定な化学種に変化したもので、細胞や組織に損傷を与える可能性がある。抗酸化物質によって通常は中和される。
*5 アストロサイト:脳や脊髄の神経細胞をサポートし、栄養を供給する神経膠細胞の一種。神経細胞の機能を維持するために重要な役割を果たす。
*6 全生存期間:ある疾患や治療を受けた後に、患者が生存している期間の長さを示す指標。通常、診断から治療終了までの生存期間を測定する。
*2 悪性神経膠腫:脳や脊髄の神経膠細胞から発生する非常に悪性度の高いがん。進行が早く、治療が難しいことが特徴。
*3 ミトコンドリア: 細胞内でエネルギーを生産する「発電所」のような役割を果たす小さな構造体。呼吸によって細胞が必要とするエネルギーを作り出す。
*4 活性酸素:酸素が不安定な化学種に変化したもので、細胞や組織に損傷を与える可能性がある。抗酸化物質によって通常は中和される。
*5 アストロサイト:脳や脊髄の神経細胞をサポートし、栄養を供給する神経膠細胞の一種。神経細胞の機能を維持するために重要な役割を果たす。
*6 全生存期間:ある疾患や治療を受けた後に、患者が生存している期間の長さを示す指標。通常、診断から治療終了までの生存期間を測定する。
参考文献など
[1] Sato I, Umemura M, Mitsudo K, Fukumura H, Kim J, Hoshino Y, Nakashima H, Kioi M, Nakakaji R, Sato M, Fujita T, Yokoyama U, Okumura S, Oshiro H, Eguchi H, Tohnai I, Ishikawa Y: Simultaneous hyperthermia-chemotherapy with controlled drug delivery using single-drug nanoparticles. Scientific Reports. 6:24629, 2016.
https://doi.org/10.1038/srep24629
[2] Ohtake M, Umemura M, Sato I, Akimoto T, Oda K, Nagasako A, Kim J, Fujita T, Yokoyama U, Nakayama T, Hoshino Y, Ishiba M, Tokura S, Hara M, Masuda T, Aoki I, Takemura Y, Eguchi H, Kawahara N, and Ishikawa Y: Hyperthermia and chemotherapy using Fe(Salen) nanoparticles might impact glioblastoma treatment. Scientific Reports.7, 42783, 2017.
https://doi.org/10.1038/srep42783
[3] Akimoto T, Umemura M, Nagasako A, Ohtake M, Fujita F, Yokoyama U, Eguchi H, Yamamoto T, and Ishikawa Y: Alternating Magnetic Field (AMF) Enhances Cytotoxicity of Compound C. Cancer Science. 109, 11, 3483-3493, 2018.
https://doi.org/10.1111/cas.13781
https://doi.org/10.1038/srep24629
[2] Ohtake M, Umemura M, Sato I, Akimoto T, Oda K, Nagasako A, Kim J, Fujita T, Yokoyama U, Nakayama T, Hoshino Y, Ishiba M, Tokura S, Hara M, Masuda T, Aoki I, Takemura Y, Eguchi H, Kawahara N, and Ishikawa Y: Hyperthermia and chemotherapy using Fe(Salen) nanoparticles might impact glioblastoma treatment. Scientific Reports.7, 42783, 2017.
https://doi.org/10.1038/srep42783
[3] Akimoto T, Umemura M, Nagasako A, Ohtake M, Fujita F, Yokoyama U, Eguchi H, Yamamoto T, and Ishikawa Y: Alternating Magnetic Field (AMF) Enhances Cytotoxicity of Compound C. Cancer Science. 109, 11, 3483-3493, 2018.
https://doi.org/10.1111/cas.13781
お問合せ先
横浜市立大学 広報担当
mail: koho@yokohama-cu.ac.jp
mail: koho@yokohama-cu.ac.jp

