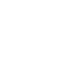大学院生の折井良太さん が筆頭著者の論文がJournal of Cell Biology に掲載!
2024.12.04
- TOPICS
- 学生の活躍
生きている細胞の新しい力学測定手法を開発することで、細胞骨格の物理的な性質を明らかにしました。
生命ナノシステム科学研究科博士後期課程2年の折井良太さんが細胞の新しい力学測定手法を開発することで、細胞骨格が物理的な力に対してどのように応答するのかを明らかにしました。その研究成果が「Journal of Cell Biology」に論文掲載されました。

筆頭著者
生命ナノシステム科学研究科 博士後期課程2年
折井 良 太さん
指導教員
生命ナノシステム科学研究科
谷本 博一 准教授(細胞生物物理学)
論文タイトル
Structural response of microtubule and actin cytoskeletons to direct intracellular load
(日本語訳:直接の力学摂動に対する微小管とアクチン骨格の構造応答)
掲載雑誌
Journal of Cell Biology
DOI: 10.1083/jcb.202403136
生命ナノシステム科学研究科 博士後期課程2年
折井 良 太さん
指導教員
生命ナノシステム科学研究科
谷本 博一 准教授(細胞生物物理学)
論文タイトル
Structural response of microtubule and actin cytoskeletons to direct intracellular load
(日本語訳:直接の力学摂動に対する微小管とアクチン骨格の構造応答)
掲載雑誌
Journal of Cell Biology
DOI: 10.1083/jcb.202403136
今回の研究内容について折井さんに解説していただきました。
細胞の力学は、主に細胞骨格である微小管*1とアクチン*2に担われています。微小管とアクチンは力に応答し、力を生成することでさまざまな生命現象を織りなします。例えば、微小管は細胞核付近を中心に放射状のネットワーク構造を形成し、モーターのような働きをするたんぱく質(分子モーター)から力を受けることで、細胞内構造の配置に寄与しています。アクチンは、フィラメント状の構造を形成して伸長することで力を生成して、細胞の運動を引き起こします。微小管とアクチンの力学的な性質を明らかにすることは生命現象の理解には必要不可欠です。
それにも関わらず、微小管とアクチンが生きている細胞の中で示す力学特性はほとんど理解されていません。細胞の外から細胞表面に力を加えることで細胞骨格の変形を引き起こす研究が古くから行われていますが、このような間接的な手法は細胞膜など、標的以外の構造の影響を受けてしまいます。生きている細胞の中で微小管やアクチンに直接力を加えて力学特性を測定する手法の構築は、生物物理学分野の大きな課題でした。
本研究は、細胞骨格の力学特性を直接測定するための新しい力学測定手法を開発しました(図a)。既存の直接測定手法の弱点である「発揮できる力が小さい」という点を克服するために、新規のプローブとして磁性流体を用いることで従来の1000倍程度の非常に大きな力の生成を可能にして、細胞骨格の変形応答を引き起こすことに成功しました。
この手法を用いて、細胞内の微小管ネットワーク構造に力を加えたところ、これまで離散的な構造であると考えられていた微小管ネットワークは、実は連続体のような変形応答を示しました(図b)。微小管の変形パターンをアクチンの変形応答と比較したことによって、微小管とアクチン構造が力学的に相互作用し、微小管構造の連続体のような応答が実現することがわかりました(図c)。さらに、微小管一本の変形応答に着目した高精度な解析により、単一高分子スケールにおいて微小管とアクチンが密接に絡まり合っていることを示しました。
本研究の成果は、細胞内構造の直接的な力学摂動に対する変形応答を定量的に測定した初めての例となります。本研究で開発した手法を用いることで、細胞骨格だけでなくさまざまな細胞内構造の力学特性の理解が進むと期待しています。
細胞の力学は、主に細胞骨格である微小管*1とアクチン*2に担われています。微小管とアクチンは力に応答し、力を生成することでさまざまな生命現象を織りなします。例えば、微小管は細胞核付近を中心に放射状のネットワーク構造を形成し、モーターのような働きをするたんぱく質(分子モーター)から力を受けることで、細胞内構造の配置に寄与しています。アクチンは、フィラメント状の構造を形成して伸長することで力を生成して、細胞の運動を引き起こします。微小管とアクチンの力学的な性質を明らかにすることは生命現象の理解には必要不可欠です。
それにも関わらず、微小管とアクチンが生きている細胞の中で示す力学特性はほとんど理解されていません。細胞の外から細胞表面に力を加えることで細胞骨格の変形を引き起こす研究が古くから行われていますが、このような間接的な手法は細胞膜など、標的以外の構造の影響を受けてしまいます。生きている細胞の中で微小管やアクチンに直接力を加えて力学特性を測定する手法の構築は、生物物理学分野の大きな課題でした。
本研究は、細胞骨格の力学特性を直接測定するための新しい力学測定手法を開発しました(図a)。既存の直接測定手法の弱点である「発揮できる力が小さい」という点を克服するために、新規のプローブとして磁性流体を用いることで従来の1000倍程度の非常に大きな力の生成を可能にして、細胞骨格の変形応答を引き起こすことに成功しました。
この手法を用いて、細胞内の微小管ネットワーク構造に力を加えたところ、これまで離散的な構造であると考えられていた微小管ネットワークは、実は連続体のような変形応答を示しました(図b)。微小管の変形パターンをアクチンの変形応答と比較したことによって、微小管とアクチン構造が力学的に相互作用し、微小管構造の連続体のような応答が実現することがわかりました(図c)。さらに、微小管一本の変形応答に着目した高精度な解析により、単一高分子スケールにおいて微小管とアクチンが密接に絡まり合っていることを示しました。
本研究の成果は、細胞内構造の直接的な力学摂動に対する変形応答を定量的に測定した初めての例となります。本研究で開発した手法を用いることで、細胞骨格だけでなくさまざまな細胞内構造の力学特性の理解が進むと期待しています。
折井 良太さんのコメント
本研究は、メインテーマの研究が行き詰ったときに着手した研究でした。試行錯誤の末に、結果として満足のいく内容になりました。
指導教官の谷本さんは、研究のけの字も知らなかった私に、熱心に指導していただきました。また研究室の方々のサポートには大変助けられました。ありがとうございます!
指導教員 谷本 博一准教授のコメント
折井くんおめでとうございます。
用語説明
*1 微小管:チューブリンと呼ばれるタンパク質が重合することで形成される一次元状の構造。高次の構造を形成することで、細胞分裂や核の中央化に寄与する。
*2 アクチン:単量体のアクチン分子が多数重合することで、アクチンフィラメントと呼ばれる一次元状の構造を形成する。細胞内ではアクチンフィラメントがさらに互いに架橋されることで密なネットワーク構造を形成する。
本研究は、メインテーマの研究が行き詰ったときに着手した研究でした。試行錯誤の末に、結果として満足のいく内容になりました。
指導教官の谷本さんは、研究のけの字も知らなかった私に、熱心に指導していただきました。また研究室の方々のサポートには大変助けられました。ありがとうございます!
指導教員 谷本 博一准教授のコメント
折井くんおめでとうございます。
用語説明
*1 微小管:チューブリンと呼ばれるタンパク質が重合することで形成される一次元状の構造。高次の構造を形成することで、細胞分裂や核の中央化に寄与する。
*2 アクチン:単量体のアクチン分子が多数重合することで、アクチンフィラメントと呼ばれる一次元状の構造を形成する。細胞内ではアクチンフィラメントがさらに互いに架橋されることで密なネットワーク構造を形成する。