新型コロナウイルスの増殖性を立体臓器「ミニ腸」で検証 〜デルタ株とオミクロン株の全く異なる特性を発見〜
2022.05.12
- プレスリリース
- 研究
- 医療
新型コロナウイルスの増殖性を立体臓器「ミニ腸」で検証
〜デルタ株とオミクロン株の全く異なる特性を発見〜
横浜市立大学大学院医学研究科 微生物学の梁 明秀教授、宮川 敬准教授、国立成育医療研究センター 生殖医療研究部の阿久津英憲部長らの研究グループは、ヒトiPS細胞由来の腸管立体臓器「ミニ腸」*1を用いて、腸管組織における新型コロナウイルス(SARS-CoV-2)変異株*2の感染性、増殖性および伝播効率について検証しました。その結果、デルタ株では腸管上皮細胞*3における顕著なウイルス増殖と、それに伴う細胞傷害性および炎症性サイトカイン*4の分泌が認められました。一方、オミクロン株 BA.1およびBA.2は腸管組織での感染・増殖効率は極めて低く、細胞傷害・炎症関連因子の上昇はほとんど見られませんでした。
このようなウイルス変異株ごとの組織・臓器レベルの感染性や増殖性の変化は、ヒト体内の感染現象を反映していると考えられ、現在流行しているオミクロン株の病態理解に役立つことが期待されます。
本研究成果は、2022年4月28日に米国消化器病学会誌「Gastroenterology」にオンライン掲載されました。
このようなウイルス変異株ごとの組織・臓器レベルの感染性や増殖性の変化は、ヒト体内の感染現象を反映していると考えられ、現在流行しているオミクロン株の病態理解に役立つことが期待されます。
本研究成果は、2022年4月28日に米国消化器病学会誌「Gastroenterology」にオンライン掲載されました。
| 研究成果のポイント ・iPS細胞から創生した機能性の立体臓器「ミニ腸」を用いて、ヒトの生体に近い状態でSARS-CoV-2変異株を感染させ、増殖効率と細胞傷害性を検証。 ・ ミニ腸において、デルタ株は従来株と比較して4〜6倍、高効率にウイルスが増殖し、隣接する複数の腸管上皮細胞間で感染クラスターを形成した。また、感染に伴う細胞傷害性や炎症性サイトカインの分泌も顕著に見られた。 ・一方、オミクロン株BA.1およびBA.2は腸管組織での感染・増殖効率は極めて低く、細胞傷害・炎症関連因子の上昇はほとんど見られなかった。 |
研究背景
SARS-CoV-2による新型コロナウイルス感染症(COVID-19)は、2年余りの間に5億人以上が罹患し、これまでに類を見ない世界的流行を示しています。主に呼吸器疾患を引き起こしますが、SARS-CoV-2は脳や腸など様々な臓器に感染することも知られています。初期の報告では、感染者は下痢症状を呈し、糞便からもウイルスが分離できることから、このウイルスは腸管にも感染して実際に複製することが示唆されていました。しかし近年、従来株よりもさらに感染伝播効率が高まったデルタ株やオミクロン株が出現しています。これらの変異株のヒトの腸管における増殖効率がどのように変化しているのかについてはこれまで知見がありませんでした。
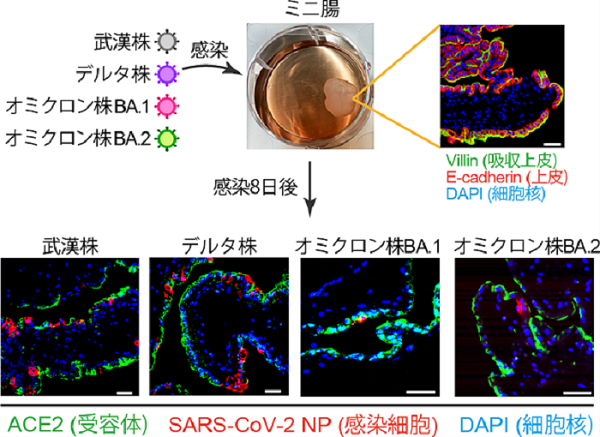
図1 SARS-CoV-2のミニ腸への感染
研究内容
ヒトiPS細胞由来の「ミニ腸」は、吸収・分泌、蠕動様運動などのヒト腸管の機能を有する機能的な立体腸管です。ミニ腸の表面にある粘膜上皮細胞ではSARS-CoV-2の侵入に必須な因子であるACE2やTMPRSS2がよく発現していました。そこで研究グループでは、武漢株、デルタ株、オミクロン株(BA.1およびBA.2)のウイルスをミニ腸に感染させ、ウイルスの増殖効率を経時的に調べました(図1)。その結果、デルタ株の増殖効率は武漢株よりも4〜6倍高いことが分かりました。一方、オミクロン株ではほとんど複製が見られませんでした(図2左)。また、武漢株やデルタ株に感染させたミニ腸では、感染に伴う細胞傷害関連分子や炎症性サイトカインの分泌が少なくとも感染8日後まで認められましたが、オミクロン株ではそのような現象は観察されませんでした。これらの結果は、デルタ株と比べてオミクロン株は腸管に感染しにくく、また感染に伴う細胞傷害や炎症も起こりにくいことを示唆しています。
デルタ株を感染させたミニ腸では、ウイルスの増殖は腸管上皮のみで観察され、粘膜下組織では観察されませんでした。また、腸管上皮では、複数の隣接する細胞群でウイルス増殖が認められましたが、単独で感染している細胞はほとんど観察されませんでした。このことは、腸管組織においてウイルスは垂直方向ではなく水平方向へ伝播することを示唆します。とくにデルタ株では、ウイルスに感染した上皮細胞は細胞融合を起こして互いに集積しており、細胞-細胞間感染*5により感染が拡大していることが示唆されました(図2右)。また、デルタ株感染後に、SARS-CoV-2に対する中和抗体*6を投与したところ、ウイルスの水平方向への拡がりが阻止されるとともに、感染細胞数が顕著に減少しました。今回の知見は、現在流行しているオミクロン株の病態理解に役立つことが期待されます。
また、今回用いたミニ腸は、生体内におけるウイルス感染ダイナミクス、および宿主応答を再現できる革新的なヒト組織系であるとともに、新たな創薬研究にも有効活用できることが分かりました。
デルタ株を感染させたミニ腸では、ウイルスの増殖は腸管上皮のみで観察され、粘膜下組織では観察されませんでした。また、腸管上皮では、複数の隣接する細胞群でウイルス増殖が認められましたが、単独で感染している細胞はほとんど観察されませんでした。このことは、腸管組織においてウイルスは垂直方向ではなく水平方向へ伝播することを示唆します。とくにデルタ株では、ウイルスに感染した上皮細胞は細胞融合を起こして互いに集積しており、細胞-細胞間感染*5により感染が拡大していることが示唆されました(図2右)。また、デルタ株感染後に、SARS-CoV-2に対する中和抗体*6を投与したところ、ウイルスの水平方向への拡がりが阻止されるとともに、感染細胞数が顕著に減少しました。今回の知見は、現在流行しているオミクロン株の病態理解に役立つことが期待されます。
また、今回用いたミニ腸は、生体内におけるウイルス感染ダイナミクス、および宿主応答を再現できる革新的なヒト組織系であるとともに、新たな創薬研究にも有効活用できることが分かりました。
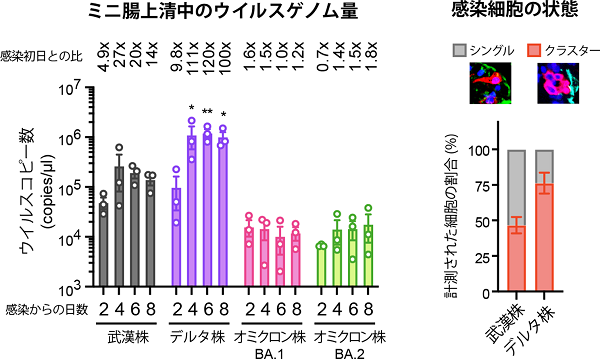
図2 ミニ腸におけるSARS-CoV-2の増殖と感染細胞の状態
今後の展開
本研究では生体に近い立体臓器を用いることで、SARS-CoV-2の感染の拡がり方を多角的に捉えることに成功しました。今後、この知見を病態解明や創薬研究に応用していきたいと考えています。また、オミクロン株は、デルタ以前の株に比べてウイルスが大きく変異しており、このことが腸管での感染が起こりにくい要因の一つと考えられます。
論文情報
タイトル: Reduced replication efficacy of SARS-CoV-2 Omicron variant in “mini-gut” organoids.
著者: Kei Miyakawa, Masakazu Machida, Tomoyuki Kawasaki, Mayuko Nishi, Hidenori Akutsu*, Akihide Ryo*
掲載雑誌:Gastroenterology
DOI:10.1053/j.gastro.2022.04.043
著者: Kei Miyakawa, Masakazu Machida, Tomoyuki Kawasaki, Mayuko Nishi, Hidenori Akutsu*, Akihide Ryo*
掲載雑誌:Gastroenterology
DOI:10.1053/j.gastro.2022.04.043
用語説明
*1 ミニ腸 : 国立成育医療研究センターの阿久津英憲部長らが2017年に開発した、ヒトiPS細胞より創生した小腸の立体臓器モデル。栄養吸収をおこなう粘膜上皮および粘膜下組織、その外側に筋肉や独立した神経系があり、ペプチドホルモンなどを分泌しながら、自律的に制御、調和しながら動いている。小腸の立体臓器モデルは、他の研究グループでも開発されているが、腸上皮が外側に配向していて、液体培地で培養できるのは、今回用いたミニ腸の大きな特徴である。
《参考》https://www.ncchd.go.jp/press/2017/es-organoid.html
*2 SARS-CoV-2変異株 : 一般的に、ウイルスは感染や増殖を繰り返すうちに徐々に変異が入る。ここでは2022年4月現在、WHOが「懸念される変異株(VOC)」として定めているデルタ株とオミクロン株(BA.1およびBA.2系統)について調べた。
*3 腸管上皮細胞 : 腸管の組織を細菌から守るための粘膜バリアを構築する細胞で、栄養や水分の吸収機能も担う。
*4 炎症性サイトカイン : 炎症の重要な調節因子で細胞から分泌されるタンパク質の総称。
*5 細胞-細胞間感染 : 感染細胞が隣接した非感染細胞にウイルスを直接受け渡す感染伝播様式。
*6 中和抗体 : ウイルスを取り巻くスパイクタンパク質に結合する抗体のうち、感染を阻止する能力をもつ抗体のこと。治療薬として用いられている。
《参考》https://www.ncchd.go.jp/press/2017/es-organoid.html
*2 SARS-CoV-2変異株 : 一般的に、ウイルスは感染や増殖を繰り返すうちに徐々に変異が入る。ここでは2022年4月現在、WHOが「懸念される変異株(VOC)」として定めているデルタ株とオミクロン株(BA.1およびBA.2系統)について調べた。
*3 腸管上皮細胞 : 腸管の組織を細菌から守るための粘膜バリアを構築する細胞で、栄養や水分の吸収機能も担う。
*4 炎症性サイトカイン : 炎症の重要な調節因子で細胞から分泌されるタンパク質の総称。
*5 細胞-細胞間感染 : 感染細胞が隣接した非感染細胞にウイルスを直接受け渡す感染伝播様式。
*6 中和抗体 : ウイルスを取り巻くスパイクタンパク質に結合する抗体のうち、感染を阻止する能力をもつ抗体のこと。治療薬として用いられている。