ポリジェニックリスクスコアで、薬剤性肝障害の感受性を規定する~ゲノムから疾患のなりやすさを予測する~
2020.09.08
- TOPICS
- 研究
- 医療
ポリジェニックリスクスコアで、薬剤性肝障害の感受性を規定する
~ゲノムから疾患のなりやすさを予測する~
| 研究成果のポイント ・ 2万以上の遺伝的多型*1から算出したPRS (ポリジェニックリスクスコア)*2がDILI (薬剤性肝障害)*3の遺伝的感受性を予測しうることを示しました。 ・ヒトiPS細胞由来肝オルガノイド*4、ヒト肝細胞を用いた検討から、DILIの感受性は酸化ストレスや小胞体ストレスなどのメカニズムに関連することを明らかにしました。 ・薬剤開発段階においてDILIの予測精度の高い前臨床試験・臨床試験の実現に貢献します。 ・ゲノム情報の明らかなヒト細胞とポリジェニックリスクスコアを組み合わせる「Polygenicity in a dish」と呼ぶ新しい研究戦略によって、さまざまな疾患に対する個別化医療・予防医療への展開が期待されます。 |
東京医科歯科大学統合研究機構の武部貴則教授の研究グループ(研究開始時の所属、横浜市立大学)は、武田薬品工業株式会社と京都大学iPS細胞研究所 (CiRA)の共同研究プログラムであるT-CiRA Joint Program*5の一環として、個人のゲノム情報から算出したPRS (ポリジェニックリスクスコア)がDILI (薬剤性肝障害)の罹患感受性を予測しうることをヒトiPS細胞由来肝オルガノイド、ヒト肝細胞、臨床データを用いて示しました。今後、薬剤開発の主要な終了要因の一つであるDILIを精度高く予測できる前臨床試験の開発や、PRSを活用することで被験者のDILIリスクを加味した臨床試験のデザインにつながります。さらに、この研究によって提唱された、ゲノム情報の明らかなヒト細胞とPRSを組み合わせる「Polygenicity in a dish」と呼ぶ新しい研究戦略を用いることで、DILIのみならず、さまざまな疾患に対する理解が深まり、個別化医療・予防医療への展開が期待されます。
この研究成果は、国際科学誌Nature Medicine(ネイチャーメディシン)オンライン版で発表されました。
この研究成果は、国際科学誌Nature Medicine(ネイチャーメディシン)オンライン版で発表されました。
研究の背景
薬物性肝障害(DILI)は1万人から10万人に1人が発症する稀な副作用ですが、医薬品開発プログラムや市場から薬剤が消失する最大要因になっており、第III相臨床試験における臨床試験の終了は12年間で1800億円の損失に上ると報告されています。このことから前臨床段階における高精度な医薬品候補の毒性予測が必要になっています。そこで、国際的にDILIの遺伝的感受性が存在するのかどうか検証するため、iDILIC*6やDILIN*7といった国際ゲノムコンソーシアムで取得したGWAS*8データの解析が行われているものの、予測に有益な特定の遺伝的多型を見出すことは困難でした。
こうした背景のもと本研究では、DILIの発症や進展には無数の遺伝的多型が関与していると仮説を立て、数万のリスク因子を加味したモデルであるポリジェニックリスクスコア(PRS)を算出することによって個人毎のDILI感受性の予測が可能であるか検証を行いました。すなわち、ヒトiPS細胞由来肝オルガノイド、ヒト肝細胞、臨床データを用いて、欧米のゲノムコンソーシアムで取得したGWAS*8データから構築されたPRSによるDILIの遺伝的感受性の予測可能性を検証するとともに、それらの感受性を規定していると考えられるメカニズム特定を試みました。
こうした背景のもと本研究では、DILIの発症や進展には無数の遺伝的多型が関与していると仮説を立て、数万のリスク因子を加味したモデルであるポリジェニックリスクスコア(PRS)を算出することによって個人毎のDILI感受性の予測が可能であるか検証を行いました。すなわち、ヒトiPS細胞由来肝オルガノイド、ヒト肝細胞、臨床データを用いて、欧米のゲノムコンソーシアムで取得したGWAS*8データから構築されたPRSによるDILIの遺伝的感受性の予測可能性を検証するとともに、それらの感受性を規定していると考えられるメカニズム特定を試みました。
研究成果の概要
1. 培養ヒト肝細胞の評価によりポリジェニックリスクスコアがさまざまな薬剤によるDILI感受性を層別化
まず、150種以上のDILIを発症する薬剤(DILI薬剤)に対してDILIを発症した862人のゲノムデータを用いたiDILICおよびDILINの GWAS 解析結果より、PRS に用いる遺伝的多型とリスク算出に用いる重みを決定しました。
次にヒト肝細胞およびiPS細胞由来肝オルガノイド合計26ドナーに対して、SNPアレイから取得したゲノム情報より各ドナーのPRSを算出し、DILIを発症することが報告されている薬剤12種類を処理し、実験的に生存率を評価しました。その結果、PRSと生存率は負の相関を示し、すなわちPRSの高いドナーでは軒並み生存率が低下することが示されました。26名の異なる患者に由来する培養ヒト細胞を用いて複数の薬剤での評価を行った結果、PRSによるDILIのリスク層別化はさまざまな薬剤で有効であることが示唆されました。
まず、150種以上のDILIを発症する薬剤(DILI薬剤)に対してDILIを発症した862人のゲノムデータを用いたiDILICおよびDILINの GWAS 解析結果より、PRS に用いる遺伝的多型とリスク算出に用いる重みを決定しました。
次にヒト肝細胞およびiPS細胞由来肝オルガノイド合計26ドナーに対して、SNPアレイから取得したゲノム情報より各ドナーのPRSを算出し、DILIを発症することが報告されている薬剤12種類を処理し、実験的に生存率を評価しました。その結果、PRSと生存率は負の相関を示し、すなわちPRSの高いドナーでは軒並み生存率が低下することが示されました。26名の異なる患者に由来する培養ヒト細胞を用いて複数の薬剤での評価を行った結果、PRSによるDILIのリスク層別化はさまざまな薬剤で有効であることが示唆されました。
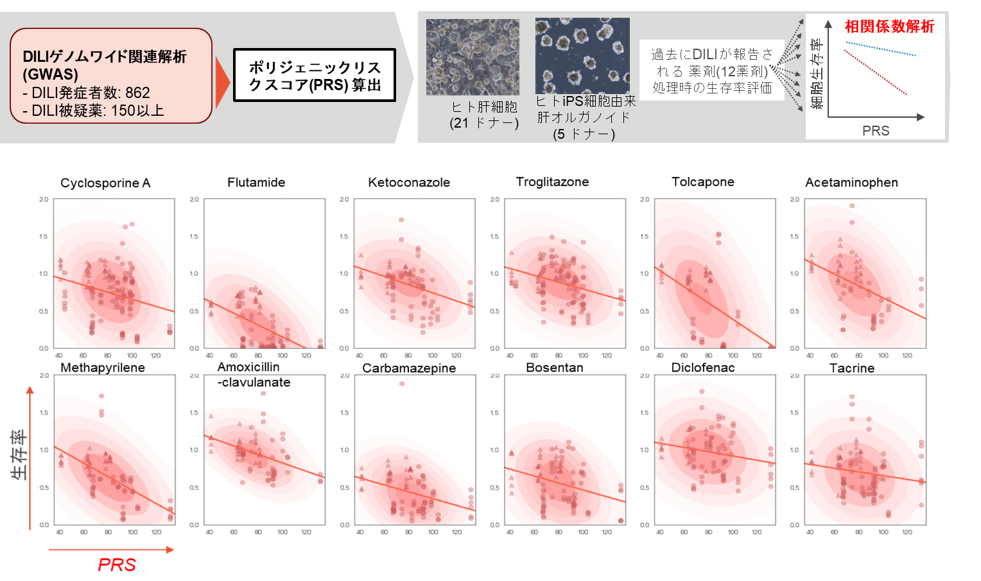
図1. DILI薬剤処理時の生存率とPRSの相関比較
2. 臨床試験データの再解析によりポリジェニックリスクスコアがDILI感受性を層別化
次に、PRSを算出したGWASとは独立した臨床試験データで、臨床でのDILIの予測が可能かを調べました。DILIは障害を受ける細胞によって、胆汁うっ滞・混合型DILI (CM-DILI), 肝細胞障害型DILI(HC-DILI)と大きく2つに分類されます。今回、特に CM-DILIの患者のGWASからそれぞれPRSに用いる遺伝的多型とリスク算出に用いる重みを決定し、Fasiglifam、Flucloxacillin、およびAmoxicillin-ClavulanateによりDILIを発症した臨床試験データで、PRSがコントロール群とDILI発症群を分けることができるか検討しました。その結果、CM-DILIのGWASを基に算出されたPRSでのみコントロール群とDILI発症群とで有意差を示しました。患者のデータによっても、PRSによるDILI感受性予測が可能であることが示唆されました。
次に、PRSを算出したGWASとは独立した臨床試験データで、臨床でのDILIの予測が可能かを調べました。DILIは障害を受ける細胞によって、胆汁うっ滞・混合型DILI (CM-DILI), 肝細胞障害型DILI(HC-DILI)と大きく2つに分類されます。今回、特に CM-DILIの患者のGWASからそれぞれPRSに用いる遺伝的多型とリスク算出に用いる重みを決定し、Fasiglifam、Flucloxacillin、およびAmoxicillin-ClavulanateによりDILIを発症した臨床試験データで、PRSがコントロール群とDILI発症群を分けることができるか検討しました。その結果、CM-DILIのGWASを基に算出されたPRSでのみコントロール群とDILI発症群とで有意差を示しました。患者のデータによっても、PRSによるDILI感受性予測が可能であることが示唆されました。
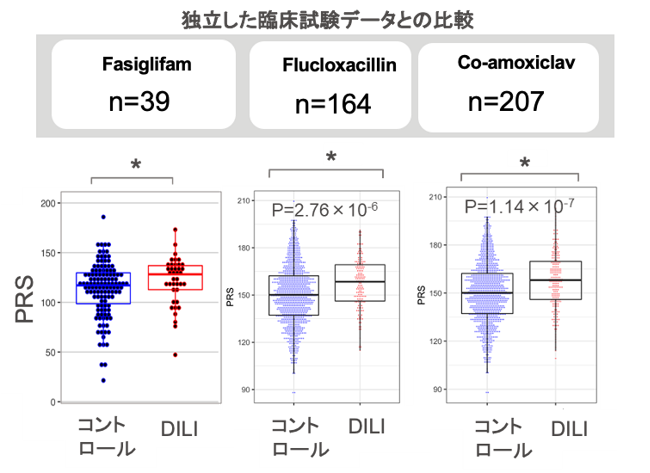
図2. 各種薬剤のDILI患者におけるPRSの分布
3. ポリジェニックリスクスコアは小胞体ストレスや酸化ストレスに関連
PRSを規定する遺伝的多型*1近傍には、酸化ストレス、ERストレス、ミトコンドリア活性に関連する遺伝子群が多く集積していることが判明しました (図3A)。 そこで、DILIの感受性に関連するメカニズムを検討するため、PRSでDILIリスクを予測したiPS細胞由来肝オルガノイドを用いてDILI薬剤処理下の遺伝子発現解析、機能解析を行いました。ヒトiPS細胞由来肝オルガノイドのDILI薬剤処理下の遺伝子発現解析では、PRSが高いほどミトコンドリア活性に関する遺伝子発現が減少し、ERストレス関連遺伝子の発現が増加する傾向が得られました(図3B)。さらに、抗酸化剤であるバルドキソロンを添加することでPRSが特に高いドナー由来のiPS細胞由来肝オルガノイドで生存率が大幅に回復したことから(図3C)、DILIの遺伝的リスクの高いドナーがDILIを発症した際の酸化ストレスの関与が実験的にも示されました。以上より、 DILI感受性に関連するメカニズムの一端が解明され、今後抗酸化剤を処置するといったDILIの予防対策も取りうる可能性が示唆されました。
PRSを規定する遺伝的多型*1近傍には、酸化ストレス、ERストレス、ミトコンドリア活性に関連する遺伝子群が多く集積していることが判明しました (図3A)。 そこで、DILIの感受性に関連するメカニズムを検討するため、PRSでDILIリスクを予測したiPS細胞由来肝オルガノイドを用いてDILI薬剤処理下の遺伝子発現解析、機能解析を行いました。ヒトiPS細胞由来肝オルガノイドのDILI薬剤処理下の遺伝子発現解析では、PRSが高いほどミトコンドリア活性に関する遺伝子発現が減少し、ERストレス関連遺伝子の発現が増加する傾向が得られました(図3B)。さらに、抗酸化剤であるバルドキソロンを添加することでPRSが特に高いドナー由来のiPS細胞由来肝オルガノイドで生存率が大幅に回復したことから(図3C)、DILIの遺伝的リスクの高いドナーがDILIを発症した際の酸化ストレスの関与が実験的にも示されました。以上より、 DILI感受性に関連するメカニズムの一端が解明され、今後抗酸化剤を処置するといったDILIの予防対策も取りうる可能性が示唆されました。
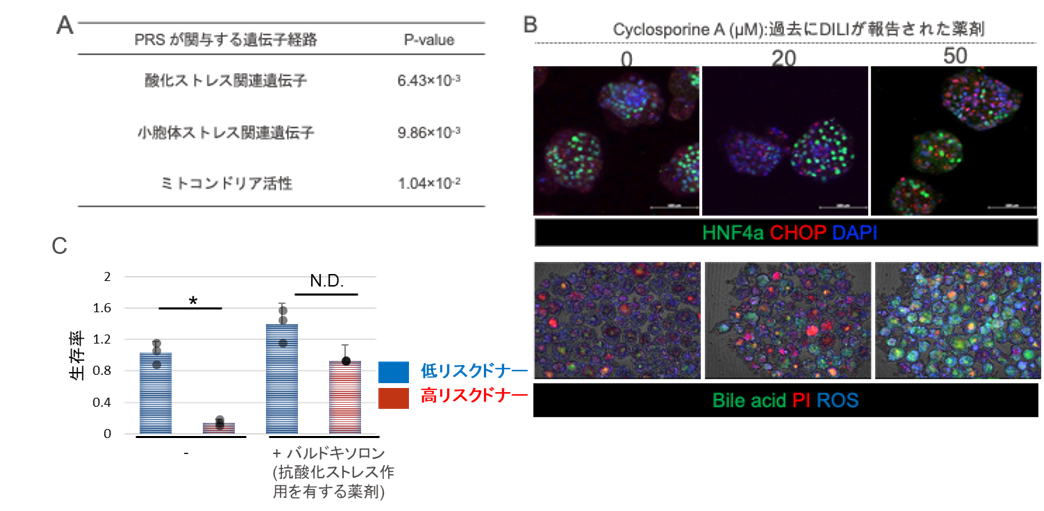
図3. DILIの感受性に関連するメカニズムの解析
A: PRSに関連する遺伝子経路の評価
B: ヒトiPS細胞由来肝オルガノイドにおけるDILI薬剤処理下の蛍光染色。上段は小胞体ストレスを、下段は酸化ストレスを示す。
C: ヒトiPS細胞由来肝オルガノイドにおけるDILI薬剤および抗酸化剤処理下の生存率の比較
研究成果の意義
- 本研究では、DILIがPRSによって予測できることを遺伝子、細胞、オルガノイド、ヒト臨床研究データを用いて初めて示しました。
- iPS細胞を用いる利点を活用し、PRSが紐づいたiPS細胞由来肝オルガノイドパネルを毒性・創薬スクリーニングに応用することで、個人の疾患リスクを予測した個別化治療への貢献が期待されます。
- 生活習慣病、非家族性がんおよび統合失調症などの多因子疾患の発症や進展にも、無数の遺伝的多型が関与していることが示唆されています。本論文で提案されたPRSと培養細胞を組み合わせた「Polygenicity in a dish」と呼ぶ新たな研究戦略が、さまざまな疾患研究に役に立つ可能性があります。
用語解説
*1 遺伝的多型
ゲノムのDNA配列が個人間で異なる箇所のうち、集団内で高い頻度(1%など)で存在するもの。
*2 PRS (ポリジェニックリスクスコア)
GWAS*8から得られる「1つの遺伝的多型*1が、ある疾患のリスクをどの程度予測できるか」という要約統計量を実際の個人のゲノム情報に掛け合わせることで「その遺伝的多型のみから予測される個々人の疾患リスク」が推定されるが、それをゲノム上の多数の遺伝的多型にわたって足し合わせてスコア化したもの。特定の疾患に対する個人の遺伝的発症リスクを評価します。
*3 DILI (薬剤性肝障害)
薬物が原因で起こる重大な副作用の一つで、肝臓に起こる炎症のこと。障害を受ける細胞によって、胆汁うっ滞・混合型DILI, 肝細胞障害型DILIと大別されます。
*4 オルガノイド
生体内で存在する器官に類似した組織構造体のこと。近年盛んに研究が進んでいる領域であり、武部らは2013年、2015年、2017年にさまざまな臓器のオルガノイドの作成についてNature誌(Nature 499(7459):481-4, 2013)、Cell Stem Cell誌(Cell Stem Cell, 16(5):556-65, 2015)、Cell Reports誌(Cell Reports 21, 2661–2670, 2017)に報告しています。
*5 T-CiRA(Takeda-CiRA Joint Program for iPS Cell Applications)
2015年に設立された、京都大学iPS細胞研究所(CiRA)と武田薬品の10年間の共同研究プログラムのこと。武田薬品が200億円の提携費用を提供し、CiRAの山中伸弥所長の指揮のもと、CiRA, 理化学研究所, 東京医科歯科大学の研究者のリードによりiPS細胞技術の臨床応用に向けた最先端の研究を行っています。本研究課題については、2016年11月より、横浜市立大学とT-CiRAで共同研究を開始しました(2019年1月より、武部教授が東京医科歯科大学へ転籍)。
*6 iDILIC
重篤有害事象国際コンソーシアム The International Serious Adverse Event Consortium (SAEC)がGWAS研究のために確立した英国で実施されている国際的な臨床ネットワーク。1,300以上のDILI患者の臨床情報及びゲノム情報が登録されている。International Drug-Induced Liver Network (iDILIC)の略称。
*7 DILIN
アメリカ国立衛生研究所が資金を提供する学術機関からなるコンソーシアム。DILIの診断等に役立てるために市販薬、サプリメントなどの代替薬によってDILIを発症した患者の臨床情報及びゲノム情報が登録されている。Drug-Induced Liver Injury Network (DILIN)の略称。
*8 GWAS (ゲノムワイド関連解析研究)
疾患発症や身体測定値などの個々人間の違いに影響する遺伝的多型*1を網羅的に探索する手法。ヒトを対象としたGWASでは、数千万カ所の遺伝的多型それぞれで、疾患との関連の強さや予想される影響の大きさ(疾患発症GWASであれば発症リスク)といった統計量が得られる。Genome-Wide Association Studyの略称。
ゲノムのDNA配列が個人間で異なる箇所のうち、集団内で高い頻度(1%など)で存在するもの。
*2 PRS (ポリジェニックリスクスコア)
GWAS*8から得られる「1つの遺伝的多型*1が、ある疾患のリスクをどの程度予測できるか」という要約統計量を実際の個人のゲノム情報に掛け合わせることで「その遺伝的多型のみから予測される個々人の疾患リスク」が推定されるが、それをゲノム上の多数の遺伝的多型にわたって足し合わせてスコア化したもの。特定の疾患に対する個人の遺伝的発症リスクを評価します。
*3 DILI (薬剤性肝障害)
薬物が原因で起こる重大な副作用の一つで、肝臓に起こる炎症のこと。障害を受ける細胞によって、胆汁うっ滞・混合型DILI, 肝細胞障害型DILIと大別されます。
*4 オルガノイド
生体内で存在する器官に類似した組織構造体のこと。近年盛んに研究が進んでいる領域であり、武部らは2013年、2015年、2017年にさまざまな臓器のオルガノイドの作成についてNature誌(Nature 499(7459):481-4, 2013)、Cell Stem Cell誌(Cell Stem Cell, 16(5):556-65, 2015)、Cell Reports誌(Cell Reports 21, 2661–2670, 2017)に報告しています。
*5 T-CiRA(Takeda-CiRA Joint Program for iPS Cell Applications)
2015年に設立された、京都大学iPS細胞研究所(CiRA)と武田薬品の10年間の共同研究プログラムのこと。武田薬品が200億円の提携費用を提供し、CiRAの山中伸弥所長の指揮のもと、CiRA, 理化学研究所, 東京医科歯科大学の研究者のリードによりiPS細胞技術の臨床応用に向けた最先端の研究を行っています。本研究課題については、2016年11月より、横浜市立大学とT-CiRAで共同研究を開始しました(2019年1月より、武部教授が東京医科歯科大学へ転籍)。
*6 iDILIC
重篤有害事象国際コンソーシアム The International Serious Adverse Event Consortium (SAEC)がGWAS研究のために確立した英国で実施されている国際的な臨床ネットワーク。1,300以上のDILI患者の臨床情報及びゲノム情報が登録されている。International Drug-Induced Liver Network (iDILIC)の略称。
*7 DILIN
アメリカ国立衛生研究所が資金を提供する学術機関からなるコンソーシアム。DILIの診断等に役立てるために市販薬、サプリメントなどの代替薬によってDILIを発症した患者の臨床情報及びゲノム情報が登録されている。Drug-Induced Liver Injury Network (DILIN)の略称。
*8 GWAS (ゲノムワイド関連解析研究)
疾患発症や身体測定値などの個々人間の違いに影響する遺伝的多型*1を網羅的に探索する手法。ヒトを対象としたGWASでは、数千万カ所の遺伝的多型それぞれで、疾患との関連の強さや予想される影響の大きさ(疾患発症GWASであれば発症リスク)といった統計量が得られる。Genome-Wide Association Studyの略称。
論文情報
掲載誌: Nature Medicine
論文タイトル: Polygenic architecture informs potential vulnerability to drug-induced liver injury
論文タイトル: Polygenic architecture informs potential vulnerability to drug-induced liver injury

研究者プロフィール
武部 貴則 (タケベ タカノリ) Takebe Takanori
東京医科歯科大学 統合研究機構
先端医歯工学創成研究部門 創生医学コンソーシアム 教授
横浜市立大学特別教授
・研究領域
幹細胞生物学、再生医学など
東京医科歯科大学 統合研究機構
先端医歯工学創成研究部門 創生医学コンソーシアム 教授
横浜市立大学特別教授
・研究領域
幹細胞生物学、再生医学など

小井土 大 (コイド マサル) Koido Masaru
横浜市立大学大学院医学研究科 臓器再生医学 特任助手(研究当時)
現東京大学医科学研究所 人癌病因遺伝子分野 特任助教
・研究領域
遺伝統計学、機械学習
横浜市立大学大学院医学研究科 臓器再生医学 特任助手(研究当時)
現東京大学医科学研究所 人癌病因遺伝子分野 特任助教
・研究領域
遺伝統計学、機械学習

川上 絵理 (カワカミ エリ) Kawakami Eri
武田薬品工業株式会社
T-CiRA Discovery 主任研究員
・研究領域
幹細胞生物学など
武田薬品工業株式会社
T-CiRA Discovery 主任研究員
・研究領域
幹細胞生物学など