新型コロナウイルス抗原を特異的に検出できる モノクローナル抗体の作製に成功〜国産初の抗原簡易検査キット開発を目指す〜
2020.04.20
- TOPICS
- 研究
- 医療
横浜市立大学大学院医学研究科の梁明秀教授を中心とした共同研究グループは、新型コロナウイルス(SARS-CoV-2)抗原を特異的に検出できるモノクローナル抗体の開発に成功しました。今回、作製した抗体は、近縁のSARSコロナウイルスや風邪の原因となるヒトコロナウイルスとは交差反応を示さず、新型コロナウイルス(SARS-CoV-2)だけに反応します(図1)。今後、本抗体を用いることで、簡便かつ短時間に新型コロナウイルス(SARS-CoV-2)だけを正しく検出できるイムノクロマトキットの開発を目指します。新型コロナウイルスであることを迅速に特定して即時対応ができるようになれば、適切な医療や感染の拡大阻止につながります。
| 研究成果のポイント ・ コムギ胚芽無細胞タンパク質合成法(*1)により作製した高品質な抗原を用いて、新型コロナウイルス(SARS-CoV-2)を正確に検出できるマウスモノクローナル抗体を産生するハイブリドーマ(*2)を複数株、樹立することに成功。 ・ 本抗体は、新型コロナウイルスだけに高い親和性を示し、重症急性呼吸器症候群(SARS)や中東呼吸器症候群(MERS)、およびその他の一般の風邪症状を引き起こすヒトコロナウイルスとは交差反応しない。 ・ 今後、本抗体を用いて、簡便かつ短時間に、しかも正確に新型コロナウイルス(SARS-CoV-2)が検出できるイムノクロマトキットが開発できれば、PCR法などの遺伝子検出法と比べて臨床現場の負担が軽くなり、検査数の大幅増が期待できる。 |
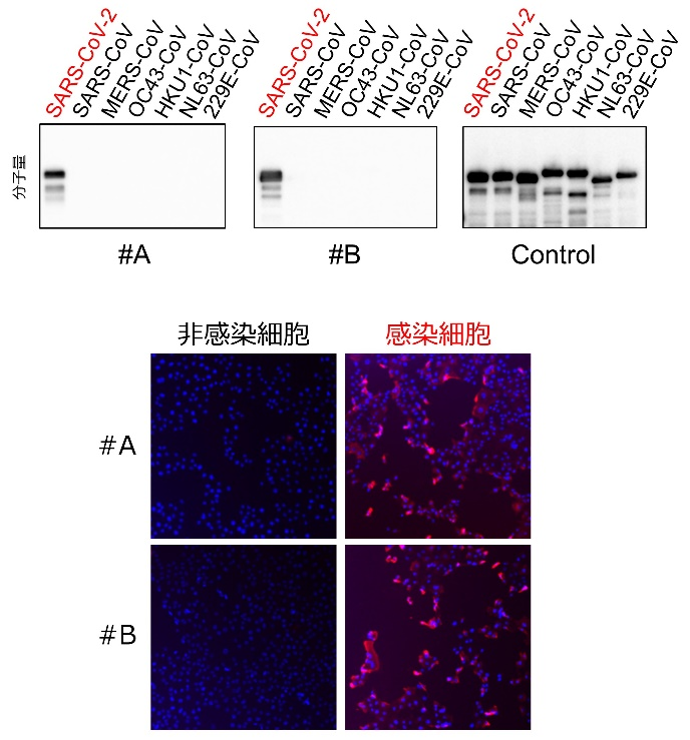
図1 抗体の性能評価
(上) ウエスタンブロットによる抗体の特異性解析。今回開発した抗体#Aおよび#Bは新型コロナウイルスのみを検出し、他のヒトコロナウイルスに交差反応しなかった。
(下) 新型コロナウイルス(SARS-CoV-2)を感染させたVero-E6/TMPRSS2細胞における蛍光免疫染色像。抗体#Aおよび#Bともに感染細胞内のウイルス抗原を検出できた。青:細胞の核、赤:ウイルス抗原
(上) ウエスタンブロットによる抗体の特異性解析。今回開発した抗体#Aおよび#Bは新型コロナウイルスのみを検出し、他のヒトコロナウイルスに交差反応しなかった。
(下) 新型コロナウイルス(SARS-CoV-2)を感染させたVero-E6/TMPRSS2細胞における蛍光免疫染色像。抗体#Aおよび#Bともに感染細胞内のウイルス抗原を検出できた。青:細胞の核、赤:ウイルス抗原
研究の背景
新型コロナウイルス感染症(COVID-19)の感染者数は200万人を超え、世界全体の死者数が16万人以上と報告されており、世界的に公衆衛生上の非常に大きな問題として早急な対策が求められています。また、本邦における感染者数も10,000例を超え、今後の感染拡大が懸念されています。現在、病原体検査は、PCR法などのウイルス遺伝子検出法のみが適用されていますが、診断までに平均約4~6時間必要とし、特殊な機器を必要とするため、検査数が限定されている状況です。医療現場で使用可能な迅速診断法として、血清抗体検出キットが開発されていますが、現在のところ、体外診断用医薬品として承認された試薬(もしくは製品)はなく、また、本法は病原体に対する免疫応答(抗体)を確認する試験法であるため、感染早期の検査には適していません。新型コロナウイルス感染症の実態を把握し、適切な感染対策と適正な医療を提供するためにも、感染早期における迅速簡易診断法の開発は緊急に進めなくてはならない課題です。一方、検査キットの開発には、新型コロナウイルス抗原を正確に認識できるモノクローナル抗体の開発が必須です。現在、使用されている抗体は、SARSコロナウイルスやその他の関連ヒトコロナウイルスなどへの交差反応が十分に検証されていないものが多く、新型コロナウイルスのみを的確に検出できる高性能なモノクローナル抗体はいまだ実用化されていません。
研究の内容
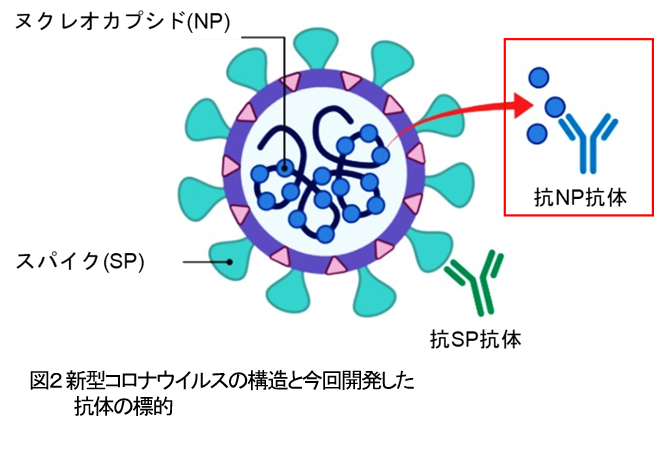
梁明秀教授を中心とした共同研究グループは、まず新型コロナウイルスを構成するヌクレオカプシドタンパク質(NP)を、梁教授の保有技術であるコムギ胚芽無細胞法を応用した病原体タンパク質合成法で大量に調製しました(図2)。次に、これを免疫原としてマウスに接種することで、NPに対するモノクローナル抗体を産生するハイブリドーマを144株樹立することに成功しました。この中から新型コロナウイルス抗原のみを特異的に認識する抗体を産生するハイブリドーマをスクリーニングしたころ、そのうちの20株が新型コロナウイルスのみを検出するモノクローナル抗体を産生していることが分かりました。
これらの抗体が認識する部位についても既に明らかにしており、各国で分離されている新型コロナウイルス株間においても保存されていることを確認しています。したがって、今回取得した抗体は、新型コロナウイルスを網羅的に検出できる優れた特性を有することが示唆されました。一方で、この認識部位は近縁のコロナウイルスとは類似性が低く、実際に本抗体は他のヒトコロナウイルスとは全く反応せず、新型コロナウイルスとのみ反応することが明らかになりました。また、バイオレイヤー干渉法技術を用いた、抗原抗体相互作用解析により、これらの抗体は抗原タンパク質であるNPに対して高い親和性を有することが分かりました。加えて、これらの抗体のうち6株は、免疫染色やELISA法(*3)などにも使用できる高品質の抗体であることがわかりました。
これらの抗体が認識する部位についても既に明らかにしており、各国で分離されている新型コロナウイルス株間においても保存されていることを確認しています。したがって、今回取得した抗体は、新型コロナウイルスを網羅的に検出できる優れた特性を有することが示唆されました。一方で、この認識部位は近縁のコロナウイルスとは類似性が低く、実際に本抗体は他のヒトコロナウイルスとは全く反応せず、新型コロナウイルスとのみ反応することが明らかになりました。また、バイオレイヤー干渉法技術を用いた、抗原抗体相互作用解析により、これらの抗体は抗原タンパク質であるNPに対して高い親和性を有することが分かりました。加えて、これらの抗体のうち6株は、免疫染色やELISA法(*3)などにも使用できる高品質の抗体であることがわかりました。
今後の展開
免疫学的手法を応用した検査キットの開発には、そのキットに用いられる抗体が病原体を正確に認識できるかどうかに依存しています。現在、まだこのキットの開発には着手できていない状況ですが、今後、この高性能な抗体を用いることで、新型コロナウイルスのみを簡単・迅速に検出できるイムノクロマトキット(*4)の開発が期待されます。ウイルス抗原タンパク質を検出できる簡易イムノキットが構築できれば、特別な装置を必要とせず、外来やベッドサイドで、簡単な操作で短時間にウイルスを検出することが可能です。今後、迅速診断法を確立し、精度の向上を図ることができれば、PCR検査との感度比較を行った上で、PCR検査前のスクリーニング検査として使用できる可能性があります。本国発の信頼性の高い簡易抗原検出キットの実用化をできるだけ早期に実現するため、臨床検査試薬の製造・販売を行う企業との連携を模索していきます。なお、開発にご関心をお持ちいただける企業様からのご連絡につきましては、下記の(製品化に関する企業様からのお問い合わせ先)にて承ります。
※本年3月9日に本学より発表しました「新型コロナウイルス抗体検出法の開発」については、精度の向上を図った上で、本年5月中旬を目処に関東化学株式会社より研究用試薬として販売予定です。また、多数の患者検体を用いた臨床性能試験を計画中であり、体外診断⽤医薬品の承認申請を早期に目指します。
※本年3月9日に本学より発表しました「新型コロナウイルス抗体検出法の開発」については、精度の向上を図った上で、本年5月中旬を目処に関東化学株式会社より研究用試薬として販売予定です。また、多数の患者検体を用いた臨床性能試験を計画中であり、体外診断⽤医薬品の承認申請を早期に目指します。
用語説明
*1 コムギ無細胞タンパク質合成法:
タンパク質合成阻害物質を除去した小麦胚芽抽出液に、アミノ酸などの基質と目的mRNAを加えるだけで、安定・効率的にタンパク質を合成する技術。本手法を用いることで従来合成が困難とされてきたウイルスタンパク質の大量合成が可能となる。
*2 ハイブリドーマ:
抗体を作り出すB細胞と、無限に増え続ける能力を持ったミエローマ細胞を融合した細胞。この細胞は増殖しながら抗体を多く産生するので、モノクローナル抗体を多量に得ることができる。
*3 ELISA法(Enzyme-Linked Immuno Sorbent Assay):
抗原または抗体を使った免疫学的測定法の1つ。試料溶液中に含まれる目的の抗原または抗体を、特異抗体あるいは抗原で捕捉し、酵素反応を利用して検出および定量を行う。
*4 イムノクロマト法:
抗原抗体反応と毛細管現象を応用した免疫測定試薬。簡単な操作で病原体などを目視で検出することが可能であり、既にインフルエンザウイルスや妊娠診断などで実用化されている。
タンパク質合成阻害物質を除去した小麦胚芽抽出液に、アミノ酸などの基質と目的mRNAを加えるだけで、安定・効率的にタンパク質を合成する技術。本手法を用いることで従来合成が困難とされてきたウイルスタンパク質の大量合成が可能となる。
*2 ハイブリドーマ:
抗体を作り出すB細胞と、無限に増え続ける能力を持ったミエローマ細胞を融合した細胞。この細胞は増殖しながら抗体を多く産生するので、モノクローナル抗体を多量に得ることができる。
*3 ELISA法(Enzyme-Linked Immuno Sorbent Assay):
抗原または抗体を使った免疫学的測定法の1つ。試料溶液中に含まれる目的の抗原または抗体を、特異抗体あるいは抗原で捕捉し、酵素反応を利用して検出および定量を行う。
*4 イムノクロマト法:
抗原抗体反応と毛細管現象を応用した免疫測定試薬。簡単な操作で病原体などを目視で検出することが可能であり、既にインフルエンザウイルスや妊娠診断などで実用化されている。
※本研究は、国立研究開発法人日本医療研究開発機構(AMED)の新興・再興感染症に対する革新的医薬品等開発推進研究事業「新型コロナウイルス感染症(COVID-19)の診断法開発に資する研究 (研究代表者:国立感染症研究所 感染病理部 鈴木忠樹部長)」の支援を受けて行われました。また、抗体の開発およびスクリーニングは関東化学株式会社との共同研究として実施されました。
お問合わせ先
以下、メールアドレスにご連絡をお願い致します。
(取材等に関するお問い合わせ)
E-mail:kenkyupr@yokohama-cu.ac.jp
(製品化に関する企業様からのお問い合わせ)
E-mail:sanren@yokohama-cu.ac.jp