腸管粘膜バリア機能に着目した新たな動脈硬化治療 ~『PLOS ONE』に掲載~
- プレスリリース
- 研究
- 医療
腸管粘膜バリア機能に着目した新たな動脈硬化治療
~『PLOS ONE』に掲載~
研究成果のポイント
|
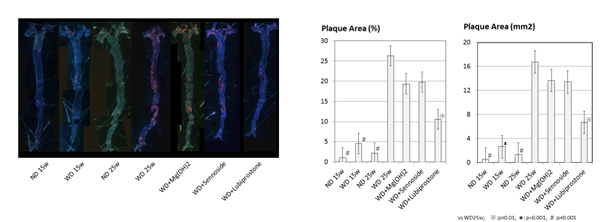
Lubiprostoneを投与すると、動脈硬化性プラークが抑制される(WD+Lubiprostone)。
(右図)プラーク面積の比率(%)と絶対値(mm2)について比較検討すると、統計学的に有意差が認められる。
研究の背景
動脈硬化症は生活習慣病(高血圧、糖尿病、脂質異常症)の終末像です。特に症状のないまま、気がつかない間に進行し、急激に心臓や、脳、腎臓などの重要臓器の障害というかたちで発症します。膨大な医療資源(人的、時間的、経済的コスト)を費やした急性期治療により、救命を果たしたとしても、重篤な後遺症により社会生活から脱落するリスクを持つ重大な疾患です。潜在患者数は国内だけでも高血圧症約4000万人、糖尿病約800万人、脂質異常症約2200万人に達し、本邦の死亡原因の第2位、第3位を占める心疾患、脳血管障害の死亡の大部分は、動脈硬化症が基盤となって起こったものであり、年間死亡者は約35万人に達すると推定されています。平成25年度の心臓病の死亡率は、人口10万対157.9であり、生活習慣病の増加を背景に年々右肩上がりに増加しており(年平均約2%:平成7年~)、今後も増加すると予測され、その早期診断や予防技術の開発が待たれています。
生活習慣病(高血圧、糖尿病、脂質異常症)の診断・治療は大きく進歩し、適切に治療することができるようになりました。しかし、生活習慣病を治療している間も、動脈硬化症は進展します。そのために、動脈硬化症診療において、残余リスク*2といわれる、未知の病態の解明と、その克服が求められています。これまでに石上准教授のグループは、動脈硬化症に関与する自己抗体の解明(Ishigami T et al, FASEB J, 2013, 国内外特許取得)、ならびに腸内共生微生物による脾臓由来のB2細胞サブセットの活性化の解明とその制御による動脈硬化症の制圧(Chen L, Ishigami T, et al. EBioMedicine, 2016、国内外特許申請中)に取り組んできました。不適切な食生活によって、腸内細菌が体内に取り込まれることによって、脾臓にあるB細胞が活性化され、IgG/IgG3という抗体を分泌することで、動脈硬化症が発症すると考えられます。このたびの本研究では、腸内細菌が体内に取り込まれる機序、腸内バリアといわれる防御機構が破綻するメカニズムに注目しました。クロライド・チャネル活性化剤Lubiprostoneは、腸上皮に作用して、腸管バリアのひとつである、粘液の産生を促すことが知られています。Lubiprostoneによる、腸管バリア機能の修復により、動脈硬化症の進展が抑制される可能性があります。本研究では遺伝性脂質異常モデルであるApoEノックアウトマウスを対象にして、検討しました。
研究の内容
本研究ならびにこれまでの研究により、動脈硬化症には、腸内細菌の抗原化による脾臓由来B2細胞サブセットの活性化とともに、腸管粘膜のバリア機能の障害といった病態があり、新規のクロライド・チャネル活性化剤であるLubiprostoneが、こうした病態を修正し、抗動脈硬化作用を発揮する可能性を明らかにすることができました。
今後の展開
用語解説
*2 残余リスク(RR: residual risk):高血圧、脂質異常症、糖尿病、喫煙は動脈硬化症の4大リスクとして知られていました。リスクは原因ではないので、リスク対策により、動脈硬化症の発症の確度を抑制することはできますが、制圧・克服までには至りません。近年、動脈硬化症における炎症という病態が、4大リスクとは異なる病態として解明が待たれています。本研究では、炎症をもたらす基盤に、食生活・B細胞・抗体がかかわるとともに、健康的な腸管バリアの維持が、重要であることを明らかにすることができました。
※本研究は、『PLOS ONE』に掲載されました( 6月17日付オンライン)。
Lubiprostone as a potential therapeutic agent to improve intestinal permeability and prevent the development of atherosclerosis in apolipoprotein E-deficient mice
Kentaro Arakawa, Tomoaki Ishigami , Michiko Nakai-Sugiyama, Lin Chen, Hiroshi Doi, Tabito Kino, Shintaro Minegishi, Sae Saigoh-Teranaka, Rie Sasaki-Nakashima, Kiyoshi Hibi, Kazuo Kimura , Kouichi Tamura
PLOS ONE June 17, 2019https://doi.org/10.1371/journal.pone.0218096
※本研究は、文部科学省科学研究費補助金、横浜市経済局・横浜ライフイノベーションプラットフォーム(LIP.横浜)の支援を受け実施されました。
お問い合わせ先
医学部 循環器・腎臓・高血圧内科学
准教授 石上友章 E-mail: tommmish@yokohama-cu.ac.jp
TEL: 045-787-2635 FAX: 045-701-3738
(取材対応窓口、資料請求など)
研究企画・産学連携推進課
課長 渡邊 誠 E-Mail: kenkyupr@yokohama-cu.ac.jp
TEL: 045-787-2510