DNAの「ねじれ」を解消し、抗がん剤の標的として重要なタンパク質の新機能を解明
- TOPICS
- 研究
- 医療
DNAの「ねじれ」を解消し、抗がん剤の標的として重要なタンパク質の新機能を解明
細胞内でDNAの「ねじれ」や「からまり」を解消する役割を担っているタンパク質「DNAトポイソメラーゼIIβ」は、エトポシドやドキソルビシンといった抗癌剤の標的分子であることからがん治療において重要な分子です。本研究グループは、パルスレーザーを使用して細胞中の狙った部位にDNAの切断を作り出す技術を利用することで、生きている細胞の中でDNA切断が生じるとDNAトポイソメラーゼIIβが素早く応答して切断部位に秒単位で集まる様子を観察することに成功しました。次にDNAトポイソメラーゼIIβの遺伝子を破壊したヒト細胞を作製したところ、この細胞はDNA損傷剤ブレオマイシンに対する感受性が上がり、DNA切断の修復メカニズムの一つである相同組換えの効率が低下していることを明らかにしました。本研究はDNAトポイソメラーゼIIβがDNA切断に素早く応答してその修復に関与することを世界で初めて示す成果であるとともに、このタンパク質を標的とするがん治療の効率化や副作用低減を考える上で重要な新知見といえます。
本研究の成果は平成30年7月9日に「Scientific Reports」に掲載されました。本研究は熊本大学パルスパワー科学研究所共同研究として実施されました。また文部科学省科学研究費補助金の支援を受けました。
論文情報
タイトル:Dynamic behavior of DNA topoisomerase IIβ in response to DNA double-strand breaks.
著者:Keiko Morotomi-Yano1, Shinta Saito2, Noritaka Adachi2, 3, Ken-ichi Yano1(責任著者)
所属:1 熊本大学 パルスパワー科学研究所、2 横浜市立大学大学院生命ナノシステム科学研究科、3 横浜市立大学 先端医科学研究センター
掲載誌:Scientific Reports
DOI:10.1038/s41598-018-28690-6.
URL:http://www.nature.com/articles/s41598-018-28690-6
説明
生命の設計図であるDNAは二本の鎖が撚(よ)り合わさった二重らせん構造をとっています。DNAが複製されて細胞分裂とともに二つに分配される際や、DNAからの情報の読み出しである転写反応の際に、過剰な「ねじれ」などの立体構造のひずみが生じることがあります。DNAトポイソメラーゼIIと呼ばれるタンパク質は、DNAを一時的に切断して立体構造のひずみを解消し、すぐに再結合することでDNAを通常の立体構造に戻すことができるため、DNAの複製や細胞の増殖にとって重要な働きをしています。
DNAトポイソメラーゼIIの働きを阻害する様々な化合物が知られていますが、その中でもエトポシドやドキソルビシンは、DNAトポイソメラーゼIIが作り出した一時的なDNA切断が再結合されることを妨げることで、DNA鎖の完全な切断であるDNA二重鎖切断を作り出します。細胞にとってDNA二重鎖切断は最も重い障害の一つであり、過剰なDNA二重鎖切断の生成は細胞死を引き起こします。そこでこれらの化合物は抗がん剤として広く用いられています。
DNAトポイソメラーゼIIは、エトポシドなどによるDNA二重鎖切断生成の標的として重要であることは広く認知されてきましたが、別の要因でDNA二重鎖切断が生じたときに何らかの生理的な役割を担っているかについては長らく不明でした。そこで本研究グループは生きている細胞内でDNA二重鎖切断が生じた場合に、DNAトポイソメラーゼIIの細胞内でのふるまいに何か変化が生じないかについて調べることから研究をスタートしました。
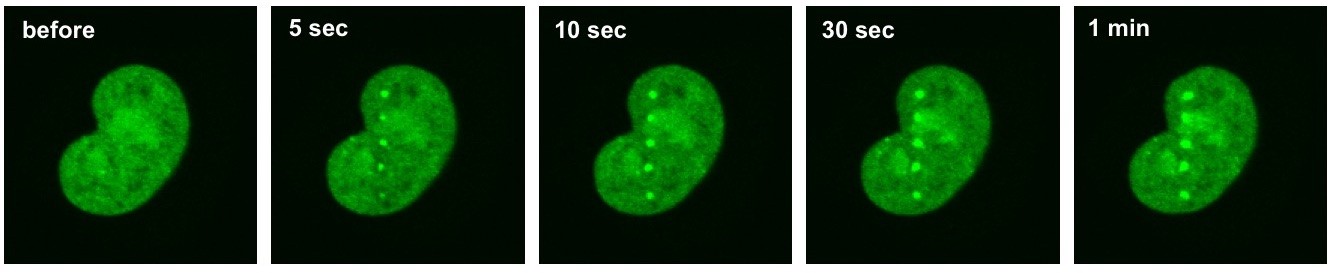
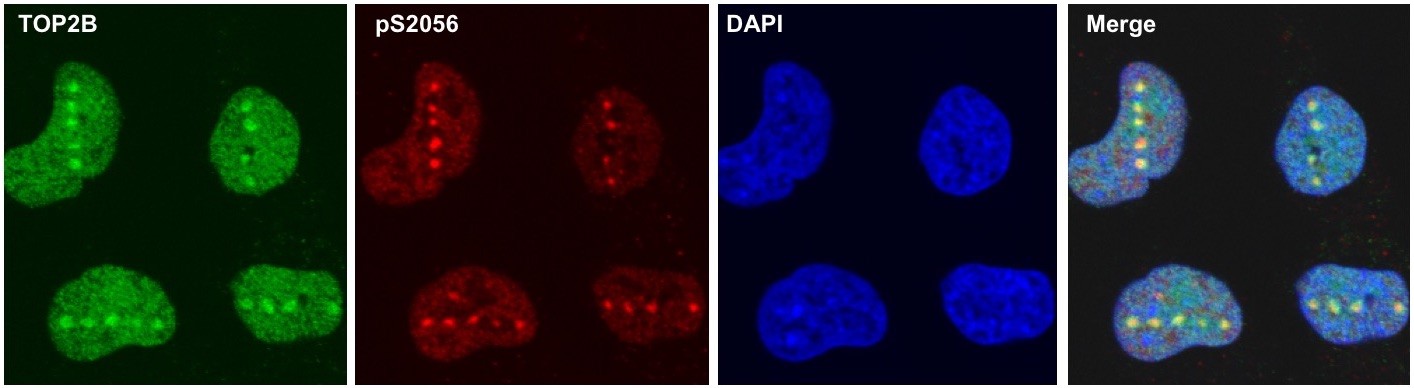
ヒト細胞が持つ二つのDNAトポイソメラーゼII(αとβ)のうち、DNAトポイソメラーゼIIβ(Topo IIβ)を研究対象に選びました。 Topo IIβに蛍光タンパク質を結合させることでTopo IIβの細胞内挙動を顕微鏡下で観察できるよう可視化しました。続いて顕微鏡観察中の生きた細胞の中の任意の一点にパルスレーザーを照射して、そこにDNA二重鎖切断を人為的に作り出せるようにしました。その結果、DNA二重鎖切断が生じるとTopo IIβが秒単位のスピードで切断部位に素早く集まってくることが生きた細胞の中で観察されました。さらに、生きた細胞内でのタンパク質の動きを解析する手法(FRAP法)によって、Topo IIβが細胞核内で激しく動き回っていることが観察され、薬物によりこの動きを止めるとDNA二重鎖切断への応答も停止することがわかりました。また切断部位にTopo IIβが集まるためには、その周辺のクロマチンタンパク質の化学修飾(アセチル化とポリADPリボース化)が重要であることも見出しました。以上の観察は、重篤な細胞障害であるDNA二重鎖切断にTopo IIβが素早く応答することを世界で初めて示すものです。
次に遺伝子ノックアウト技術によりTopo IIβタンパク質を産生しないヒト細胞を作製したところ、この細胞はDNA損傷剤であるブレオマイシンに対して高感受性であることがわかりました。続いてDNA二重鎖切断の主要な修復メカニズムである相同組換えの効率を定量的に測定するためのレポーター遺伝子を染色体上の特定部位にノックインした細胞を作製しました。この細胞を用いた解析により、Topo IIβタンパク質を産生しないヒト細胞では相同組換えを介したDNA二重鎖切断の修復が顕著に低下していることを明らかにしました。
以上の一連の新知見はTopo IIβがDNA二重鎖切断に素早く応答して、相同組換えを介した修復に関与することを世界で初めて示したものです。またエトポシドやドキソルビシンといった抗がん剤によるがん治療法の効率化や、これらの抗がん剤の副作用低減を考える上での重要な新知見であり、より良いがん治療のための基盤となるものといえます。
お問い合わせ先
熊本大学パルスパワー科学研究所
教授矢野 憲一
電話:096-342-3965
e-mail:yanoken@kumamoto-u.ac.jp
【本学お問合わせ先】
大学院生命ナノシステム科学研究科
教授足立 典隆
電話:045-787-2228
e-mail:nadachi@yokohama-cu.ac.jp