血管網を有する膵島(血管化膵島)の創出に成功効率的な組織移植療法の開発へ
- TOPICS
- 研究
- 医療
血管網を有する膵島(血管化膵島)の創出に成功
効率的な組織移植療法の開発へ
~『Cell Reports』に掲載 ~
横浜市立大学 学術院医学群 臓器再生医学 谷口英樹主任教授、武部貴則教授(同大先端医科学研究センター教授・東京医科歯科大学 統合研究機構教授・シンシナティ小児病院准教授)、髙橋禎暢(研究当時大学院生)らの研究グループは、さまざまな臓器等より分離した微小な組織片を血管内皮細胞及び間葉系細胞と3次元的に共培養することで、血管網を有した立体組織を自律的に創出することに成功しました。さらに、アルバータ大学(カナダ) 金 達也教授との共同研究により、本手法をマウス・ヒト膵島*1に応用した結果、血管網を有した膵島組織を創出できること、得られた血管化膵島(新法)の移植により重症糖尿病モデルマウスの生存を大幅に改善することなどを見出しました。血管化膵島移植*2は早期の血液灌流*3を通じた膵島の構造化・機能化を促していると考えられ、治療効果に優れた新たな移植手法の確立に繋がるものと期待されます。
| 研究成果のポイント 〇さまざまな臓器の微小組織片を用いて、血管網を導入する培養系を確立 〇血管網を導入することによりマウス・ヒト膵島の機能が向上することを確認 〇血管化したマウス膵島移植により糖尿病モデルマウスの治療効果を大幅に改善 |
研究の背景
現在、重篤な1型糖尿病患者などを対象として、脳死ドナー等より分離した膵臓から血糖値の制御を担う膵島を移植することによる治療が試みられています。膵島移植は、2000年にアルバータ大学(カナダ)のグループによりEdmonton Protocolとして確立されたもので、全身麻酔や開腹手術を一切必要とせず点滴の要領で短時間に終えることが可能であるため、従来行われてきた膵臓移植などの臓器移植療法と比べ低侵襲かつ、高い安全性を備えていると考えられています。しかし、現行の方法では、膵島の抽出過程に伴って血管構造が喪失してしまうため、移植された膵島の生着効率が極めて低いことが重大な臨床的解決課題とされていました。
一方、移植膵島の血管新生を促す技術として、膵島を血管内皮前駆細胞や間葉系細胞と共移植する手法などが報告されているものの、移植後の組織に早期に血管を再構築させることはいまだ困難でした。
研究の内容と成果
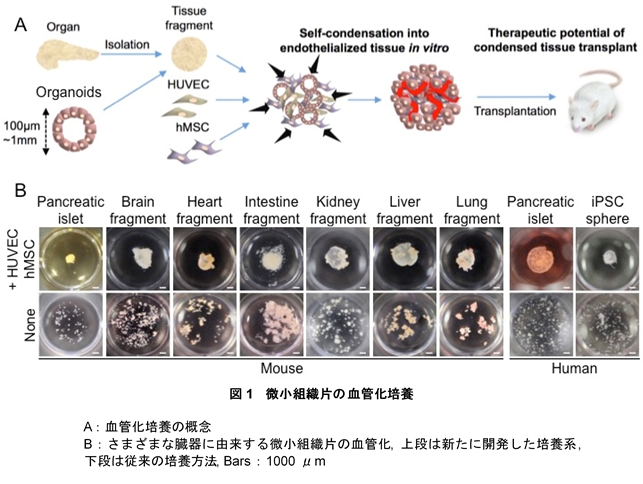
本学臓器再生医学の研究室では、ヒトiPS(人工多能性幹)細胞から分化誘導により得られた肝臓の前駆細胞を、血管内皮細胞及び間葉系幹細胞と共培養することで、従来必須と考えられていた足場材料を要することなく、in vitroで血管網を付与した立体的な肝臓原基を構築することに成功しています。本研究では、肝臓作成の領域で開発してきた血管網を再構成する基盤技術を膵島に応用し、膵島を血管内皮細胞及び間葉系細胞と3次元的に共培養し、試験管内において血管網を有する膵島(血管化膵島)を再構成するための手法を構築するとともに、劇症1型糖尿病モデルマウスを対象として新たな膵島移植(血管化膵島移植)療法の確立を試みました。ヒト(カナダ アルバータ大学より提供)及びマウス(8-12週齢C57BL/6J, CAG-EGFP)より分離した膵島組織を臍帯血静脈内皮細胞(HUVEC)、ヒト骨髄由来間葉系幹細胞(hMSC)と3次元的に共培養した結果、培地中に散乱していた細胞が自律的に凝集し血管化膵島が創出されることを発見しました(図1A)。また、興味深いことに同手法は、さまざまな臓器より抽出した組織においても応用可能であることが示されています(図1B)。
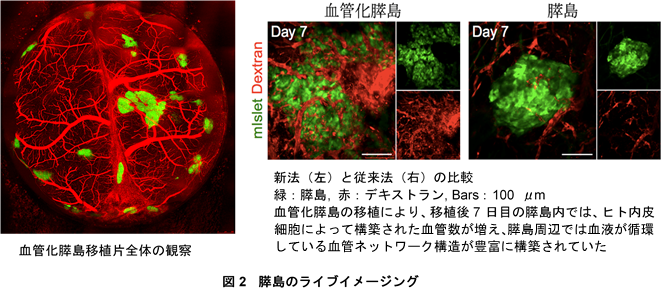
次に、血管化による膵島機能への影響を評価するためにin vitro糖負荷試験を行いました。高濃度グルコース含培地中では、膵島単独培養群と比較して共培養群において高いインスリン産生が認められました。これらの結果は、HUVEC, hMSCを用いた血管化がインスリン分泌を増強する可能性を示唆しています。さらに、このような血管化膵島を移植することにより、血管再構築が効率的に行われているか調べるため、イメージング解析を行った結果、移植後2-3日目に血管化膵島への血液再灌流が観察されました。また、血管化膵島の生着と血管新生動態を移植後0, 2, 7日目に観察したところ、2日目には複数のヒト内皮細胞が膵島内に観察されました。移植7日目の膵島内では、ヒト内皮細胞によって構築された血管数が増え、膵島周辺では血液が循環している血管ネットワーク構造が豊富に構築されていました(図2)。
膵島単独移植群では、膵島内の血液再灌流や形態的変化が観察されず、生存している膵島数は経時的に減少しました。これらの結果から、血管化膵島移植によって早期血液灌流誘導が達成されることが示されました。また移植片の組織学的解析の結果、血管化膵島は単に基底膜を伴って安定した血管構造を持っているだけでなく、膵αやβ細胞等の膵島細胞や他の内分泌成分を保持することで、正常な生理機能を持った構造を維持しているものと示唆されました。
最終的に、血管化膵島移植による糖尿病治療効果を検証するため、免疫不全1型糖尿病モデルマウスを作製し、腎被膜下に血管化膵島を移植し、生存率、体重、血糖値の推移を測定しました。移植5日目、対照マウスのほとんどは死亡したのに対し、膵島を単独(従来法)移植した糖尿病マウスの生存率は40%でした。しかしながら、血管化膵島(新法)を移植したマウスは、90%以上が生存していました。また、移植後、血管化膵島を移植したマウスは大幅な体重増加がみられ、高血糖誘発前の体重まで回復することが判明しています。これらの結果から、血管化膵島移植は早期の血液灌流を通じて生着が促され、糖尿病の治療効果を大幅に向上させているものと考えられました。
今後の展開
本研究によって、個体より分離したさまざまな器官に由来する組織片に血管内皮細胞および間葉系細胞を組み込むことにより、機能的な血管網の迅速な形成と、それにつづく自己組織化を通じた機能発現を促進できることが明らかとされました。本法は任意の種類および量の微小組織片から血管などを有した複合組織を形成するうえで汎用的な基盤技術になると考えられます。今後、このような手法を活用することで、神経や免疫細胞などいまだ評価のなされていない多様な細胞を含めた自己組織化を図ることが可能となり、さらに複雑な器官の形成を担保する新規の培養系の開発につながるものと大いに期待されます。
膵島の機能維持には豊富な血流が必要であるものの、これまで十分な血液灌流を促すことの出来る立体組織の創出は困難でした。本研究により確立された血管化膵島移植法は、移植後早期に血液再灌流を生じることで速やかな生着が担保されるばかりか、膵島機能に重要な血管基底膜の再構成や、さまざまな内分泌細胞の維持などの、複数の優位性が確保できるものと考えられます。近年、急速に研究が進んでいる、ヒトiPS細胞などを活用した膵島の作成技術と組み合わせることにより、将来的に画期的な糖尿病治療法の開発に繋がるものと期待されます。
用語説明
*2 膵島移植:何らかの原因で膵島が壊れ、インシュリンを分泌できなくなると糖尿病となり、高血糖や重症低血糖に苦しんだり、合併症の進行を防ぐことが難しくなる。そのような糖尿病患者に、臓器提供者(ドナー)より提供された膵臓から膵島細胞のみを分離して移植する治療法。膵臓移植と異なり、外科手術が不要で、患者さんの負担が軽いことが特徴。
*3血液灌流:血管を通して臓器や細胞に血液を流すこと。
掲載論文
Self-Condensation Culture Enables Vascularization Of Tissue Fragments For Efficient Therapeutic Transplantation
Takahashi, Y., Sekine, K., Kin, T., Takebe, T., and Hideki Taniguchi
Cell Reports(2018), https://doi.org/10.1016/j.celrep.2018.03.123
※本研究は、『Cell Reports』に掲載されました。(米国東部時間5月8日午前11時付:日本時間5月9日午前0時付オンライン)また、本研究のイメージが5月8日号の表紙に採用されました。
※本研究は、文部科学省科学研究費補助金 基盤研究(A)、国立研究開発法人日本医療研究開発機構(AMED)「再生医療実現拠点ネットワークプログラム」、国立研究開発法人科学技術振興機構(JST)「戦略的創造研究推進事業」の一環として、また、日本IDDMネットワークの支援を受けて行われました。
お問い合わせ先
学術院医学群臓器再生医学
主任教授谷口英樹
教授武部貴則
Tel/Fax: 045-787-8963
E-mail:rtanigu@yokohama-cu.ac.jp (谷口)
E-mail:ttakebe@yokohama-cu.ac.jp (武部)
(取材対応窓口、資料請求など)
研究企画・産学連携推進課長渡邊 誠
TEL:045-787-2510
E-Mail:kenki@yokohama-cu.ac.jp