2015.10.07
- プレスリリース
- 研究
DNAの傷を見つけたタンパク質が、修復タンパク質を呼び込むメカニズムを解明!
米国の科学雑誌『STRUCTURE』 (Cell press)誌に掲載(平成27年10月6日発行号に掲載)
筆者のアートデザインが掲載号の表紙を飾りました。
平成27年10月6日
研究推進課
研究推進課
遺伝性疾患の発症プロセス解明にも繋がる
横浜市立大学大学院生命医科学研究科 奥田昌彦特任助教と西村善文学長補佐は、神戸大学バイオシグナル研究センター 菅澤薫教授らとの共同研究で、損傷したDNAを見つけたタンパク質が、その傷を除去して治すタンパク質を呼び込むメカニズムを解明しました。
呼び込む姿は、NMRという特殊な分光器を用いて解析しました。紫外線によって傷ついたDNAを治すことができなくなると、遺伝性疾患を起こしやすくなることから、修復過程の様子を詳しく解析することは、遺伝性疾患の発症プロセス解明に繋がり、また新薬開発に役立てることが出来ます。
呼び込む姿は、NMRという特殊な分光器を用いて解析しました。紫外線によって傷ついたDNAを治すことができなくなると、遺伝性疾患を起こしやすくなることから、修復過程の様子を詳しく解析することは、遺伝性疾患の発症プロセス解明に繋がり、また新薬開発に役立てることが出来ます。
研究成果のポイント
○ 修復タンパク質を呼び込むために特定のタンパク質が働くメカニズムを解明
○ 色素性乾皮症、コケイン症候群、硫黄欠乏性毛髪発育異常症などの遺伝性疾患の治療薬の開発に貢献できる
○ DNA修復の全メカニズムの解明に繋がる
○ 色素性乾皮症、コケイン症候群、硫黄欠乏性毛髪発育異常症などの遺伝性疾患の治療薬の開発に貢献できる
○ DNA修復の全メカニズムの解明に繋がる
研究の概要と成果
私たちのDNAは、有害な代謝副産物、発癌物質、紫外線等の様々な要因により、常に損傷の危機に直面しています。重要な遺伝子が傷ついてしまうと病気を引き起こし、また傷が残ってしまうと誤った遺伝情報が次の世代に引き継がれてしまいます。しかしDNAに傷がついてしまうことを完全に回避することはできません。この重大な問題に対して私たちの身体(細胞)は、完璧な防御策を講じるよりも、ついてしまった傷を修復する素晴らしいしくみを築き上げてきました。その一つが、“ヌクレオチド除去修復”と呼ばれる仕組みで、DNA損傷部位と周辺のDNAの部品(ヌクレオチド)(*1)を除いて、新しいものに作り替えます。
ヌクレオチド除去修復において、DNAに生じた傷を最初に見つけて、修復を開始する重要な働きをするものが、XPCタンパク質です。DNAの傷を見つけた後、XPCタンパク質は、損傷周辺のヌクレオチドを切断するためにDNAの二重らせんを巻き解くタンパク質TFIIHを呼び込みます。TFIIHは、10種類の異なるタンパク質からなる大きな複合体で、普段は基本転写因子(*2)として、転写を開始するために働いていますが、DNA修復の際にも重要な役割を果たします。
本研究では、XPCタンパク質がTFIIH複合体を呼び込むために、TFIIHの構成メンバーであるp62タンパク質の結合部分(PHドメイン)と結合することを、本学のNMR(*3)を用いて解明しました(図1)。
ヌクレオチド除去修復において、DNAに生じた傷を最初に見つけて、修復を開始する重要な働きをするものが、XPCタンパク質です。DNAの傷を見つけた後、XPCタンパク質は、損傷周辺のヌクレオチドを切断するためにDNAの二重らせんを巻き解くタンパク質TFIIHを呼び込みます。TFIIHは、10種類の異なるタンパク質からなる大きな複合体で、普段は基本転写因子(*2)として、転写を開始するために働いていますが、DNA修復の際にも重要な役割を果たします。
本研究では、XPCタンパク質がTFIIH複合体を呼び込むために、TFIIHの構成メンバーであるp62タンパク質の結合部分(PHドメイン)と結合することを、本学のNMR(*3)を用いて解明しました(図1)。

研究内容の詳細
XPCタンパク質は、多くの酸性アミノ酸を含んだ約20アミノ酸の短い領域で結合していました。この領域は自身では構造を作りませんが、結合する時には伸びた紐のような構造を形成してp62のPHドメインに広く巻き付いていました。結合のしくみを詳しく調べてみると、XPCタンパク質の多くの酸性アミノ酸がp62の塩基性アミノ酸と静電的相互作用することに加えて、XPCタンパク質の酸性アミノ酸に囲まれたトリプトファンやバリン残基がp62のPHドメインのくぼみ(ポケット)に入り込むことが重要であることが分かりました。特にトリプトファンの役割は重要で、この残基をアラニンに置換した変異XPCタンパク質を細胞に導入すると、紫外線照射によって生じるDNAの傷をうまく修復出来なくなってしまいました。その原因を調べてみると、変異XPCタンパク質でも正常にDNAの損傷箇所に集まっていましたが、TFIIHはほとんど見られなくなっていました。変異XPCタンパク質がp62のPHドメインに結合できないためにTFIIHを損傷箇所に呼び寄せることが出来なくなり、修復がうまく行われなくなってしまったのです(図3)。
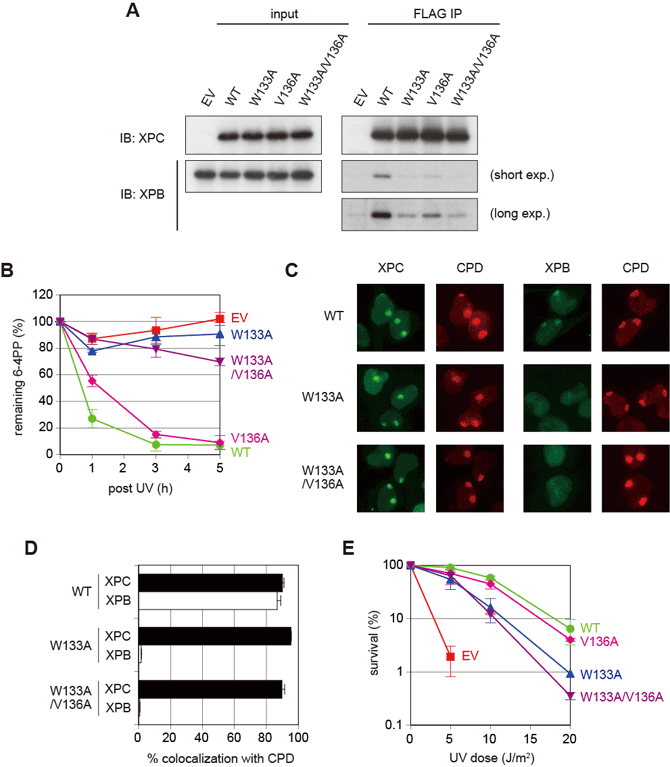
図3 XPCタンパク質がTFIIH p62のPHドメインに結合できなくなると、TFIIHをDNA損傷部位に呼び込めず、DNAの修復が出来なくなってしまうことを細胞内で明らかにした実験
最近、私たちは、がん抑制タンパク質p53やXPCタンパク質が酵素によってリン酸化される様子と、リン酸化によってp62のPHドメインに結合する様子を、同時にリアルタイムにNMRで解析する方法を確立しました(参考文献(1))。その際、XPCタンパク質の129番目のセリンのリン酸化にともなってp62 PHドメインとの結合が強まって行く中で、p62の62番目のリジンが最も大きく変化(化学シフト)することを観察しました。その理由として、セリンがリン酸化されたことで、両アミノ酸の間で静電的結合が生じたからではないかと推察していたのですが、今回の構造から両残基が空間的に近くにあることが判明し、それが正しかったことが確認できました。転写が開始される時にTFIIHを呼び込むのは同じ基本転写因子であるTFIIEαで、その酸性ドメインがp62のPHドメインを捕まえます。面白いことに、XPCの結合時の伸びた紐のような構造と、TFIIEαの酸性ドメインのアミノ末端領域の結合時の構造が類似しており、PHドメインの捕まえ方も大変よく似ていました。転写開始とDNA修復開始という異なる過程でも、TFIIHを呼び込むしくみは、とても似ていることが分かりました。
今後の展開
ヌクレオチド除去修復は、XPCタンパク質やTFIIHの他にも多くのタンパク質が関わる複雑な過程です。これらのタンパク質の遺伝子変異は、色素性乾皮症(*4)、コケイン症候群、硫黄欠乏性毛髪発育異常症などの遺伝性疾患を発症します。今回の研究ではヌクレオチド除去修復過程の最初の段階を調べました。今後は、これに続く段階でなされるタンパク質のやりとりの姿を詳しく調べ、修復メカニズムの全解明に貢献していきたいと考えております。このような研究の成果は、新薬設計に有益な情報を提供することが期待されます。
※本研究は、文部科学省「創薬等支援技術基盤プラットフォーム事業」及び「先端研究基盤共用・プラットフォーム形成事業」の研究の一環で行われました。
核酸(DNAやRNA)の構成単位。
(*2)基本転写因子
RNAポリメラーゼIIが、タンパク質合成の鋳型であるメッセンジャーRNAの合成反応を開始するのを補助するタンパク。TFIIA、TFIIB、TFIID、TFIIE、TFIIF、TFIIHの6タンパクをいう。
(*3)NMR分光器
強い磁場中で特定の原子核スピンの向きが揃えられた化合物やタンパク質等に対し、ラジオ波を照射して核磁気共鳴させた後、核スピンが元の安定な状態に戻る際に出す信号を観測して、原子の配置などを解析する装置。
(*4)色素性乾皮症
常染色体劣性遺伝性の光線過敏性皮膚疾患。
“Structural Insight into the Mechanism of TFIIH Recognition by the Acidic String of the Nucleotide Excision Repair Factor XPC”
Structure, doi:
※本研究は、文部科学省「創薬等支援技術基盤プラットフォーム事業」及び「先端研究基盤共用・プラットフォーム形成事業」の研究の一環で行われました。
参考文献
(1)M. Okuda, Y. Nishimura, Oncogenesis. e150.用語説明
(*1)ヌクレオチド核酸(DNAやRNA)の構成単位。
(*2)基本転写因子
RNAポリメラーゼIIが、タンパク質合成の鋳型であるメッセンジャーRNAの合成反応を開始するのを補助するタンパク。TFIIA、TFIIB、TFIID、TFIIE、TFIIF、TFIIHの6タンパクをいう。
(*3)NMR分光器
強い磁場中で特定の原子核スピンの向きが揃えられた化合物やタンパク質等に対し、ラジオ波を照射して核磁気共鳴させた後、核スピンが元の安定な状態に戻る際に出す信号を観測して、原子の配置などを解析する装置。
(*4)色素性乾皮症
常染色体劣性遺伝性の光線過敏性皮膚疾患。
論文著者、ならびにタイトルなど
Masahiko Okuda, Minoru Kinoshita, Erina Kakumu, Kaoru Sugasawa, Yoshifumi Nishimura“Structural Insight into the Mechanism of TFIIH Recognition by the Acidic String of the Nucleotide Excision Repair Factor XPC”
Structure, doi:
お問い合わせ先
(本資料の内容に関するお問合せ)
公立大学法人横浜市立大学大学院生命医科学研究科 特任助教 奥田 昌彦
公立大学法人横浜市立大学大学院生命医科学研究科 学長補佐 西村 善文
横浜市鶴見区末広町1‐7‐29
Tel:045-508-7211/7212
E-mail:(奥田)
(西村)
(取材対応窓口、資料請求など)
公立大学法人横浜市立大学 研究推進課長 竹内 紀充
Tel:045-787-2019
E-mail:
公立大学法人横浜市立大学大学院生命医科学研究科 特任助教 奥田 昌彦
公立大学法人横浜市立大学大学院生命医科学研究科 学長補佐 西村 善文
横浜市鶴見区末広町1‐7‐29
Tel:045-508-7211/7212
E-mail:(奥田)
(西村)
(取材対応窓口、資料請求など)
公立大学法人横浜市立大学 研究推進課長 竹内 紀充
Tel:045-787-2019
E-mail: