2013.08.01
- プレスリリース
- 研究
横浜市立大学学術院医学群 循環器・腎臓内科学 田村 功一准教授、涌井 広道助教、前田 晃延博士らは、生活習慣病の発症や進行に関わるタンパク質ATRAP/Agtrap *1 が正常なマウスやヒトの脂肪組織に多く存在し、一方、生活習慣病にかかると脂肪組織内のATRAPが減少することを明らかにしました。実際に、今回作製されたATRAP欠損マウスでは、高脂肪食での飼育下では、内臓脂肪型肥満、高血圧、脂質異常症、インスリン抵抗性(糖尿病)などの生活習慣病が出現することがわかり、さらに、ATRAPを多く発現している脂肪組織をATRAP欠損マウスに皮下移植すると生活習慣病の症状が改善できることを証明しました(図1)。
本研究は、田村准教授らが米国Harvard大学と共同で単離・同定したATRAPが、生活習慣病の病態基盤に深く関与していることを明らかにしたのみならず、生活習慣病治療における新規標的因子としての可能性を明らかにした画期的な成果です。
*1 AT1受容体結合性低分子蛋白 (AT1 receptor-associated protein; ATRAP)
本研究は、田村准教授らが米国Harvard大学と共同で単離・同定したATRAPが、生活習慣病の病態基盤に深く関与していることを明らかにしたのみならず、生活習慣病治療における新規標的因子としての可能性を明らかにした画期的な成果です。
*1 AT1受容体結合性低分子蛋白 (AT1 receptor-associated protein; ATRAP)
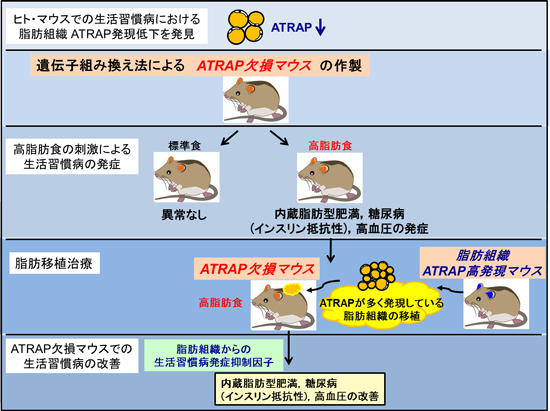 (図1)今回の研究の概要
(図1)今回の研究の概要
また、田村准教授、涌井助教、松田みゆき実験助手らは、ATRAP遺伝子の発現を増強する転写活性化因子の解析にも取り組んでおり、転写活性化に重要な発現制御領域と転写調節因子についても既に明らかにしています(『Journal of Biological Chemistry(米国生化学分子生物学会誌)』に掲載、2013年5月7日Epub)。
これらの研究成果を応用することにより、生活習慣病とその動脈硬化合併症のリスク診断や脂肪細胞移植による新規治療の実現の可能性が期待されます。
※本研究成果は、厚生労働科学研究費補助金(循環器疾患・糖尿病等生活習慣病対策総合研究事業)、日本老年医学会、日本学術振興会などの研究補助金によるものです。また、横浜市立大学先端医科学研究センターが推進している「研究開発プロジェクト」の成果のひとつです。
これらの研究成果を応用することにより、生活習慣病とその動脈硬化合併症のリスク診断や脂肪細胞移植による新規治療の実現の可能性が期待されます。
※本研究成果は、厚生労働科学研究費補助金(循環器疾患・糖尿病等生活習慣病対策総合研究事業)、日本老年医学会、日本学術振興会などの研究補助金によるものです。また、横浜市立大学先端医科学研究センターが推進している「研究開発プロジェクト」の成果のひとつです。
研究の背景
内蔵脂肪型肥満、高血圧、2型糖尿病、慢性腎臓病、脂質異常症などの生活習慣病は、遺伝的要因と後天的要因とが複雑に相互に作用し合って発症し、症状があまり顕在化しないまま増悪して動脈硬化が進行することにより、脳梗塞、心筋梗塞、腎不全、大動脈瘤、閉塞性動脈硬化症などの重篤な合併症を引き起こします。現在生活習慣病に対しては食事・運動療法に加えて種々の薬物による治療やインターベンション治療*2が行われていますが、現時点での集学的治療*3によっては完全には生活習慣病とその重篤な動脈硬化合併症を完全には抑制できないとされています。したがって、生活習慣病とその動脈硬化合併症に対する安全でさらに効率的な治療法の開発が重要とされています。
レニン-アンジオテンシン系(R-A系)はR-A系による生理作用の大部分を担う生理活性物質アンジオテンシンII (Ang II)の受容体であるAT1受容体の生理的な活性化を通じて、交感神経系などとともに、生体の血圧循環調節や腎機能制御を行っており、生体の機能維持に重要な循環調節系です。しかしながら、カロリー過剰摂取や種々のストレスなどの病的な慢性刺激により組織局所でのR-A系のAT1受容体系の過剰活性化が生じることがあり、これが原因となって組織局所での酸化ストレス増加や炎症反応が持続して引き起こされ、生活習慣病とその動脈硬化合併症の発症・進展にも深く関与することが提唱されています。したがって、生活習慣病とその動脈硬化合併症の発症・進展において、Ang II=生活習慣病増悪因子、AT1受容体=生活習慣病増悪因子受容体として捉えることができます。
一方、内蔵脂肪型肥満、インスリン抵抗性を特徴とする生活習慣病とその動脈硬化合併症においては、脂肪組織における脂肪細胞肥大化や脂肪組織での軽度な慢性炎症の病態への関与の可能性、あるいは脂肪組織でのR-A系、AT1受容体系の関与の可能性が指摘されています。しかしながらその分子病態学的な基盤については十分に解明されていませんでした。
*2 インターベンション治療: カテーテルと呼ばれる細いチューブを血管に挿入して行う治療法
*3 集学的治療: 外科的治療・内科的治療・放射線治療など複数の治療法を組み合わせて行う治療法
レニン-アンジオテンシン系(R-A系)はR-A系による生理作用の大部分を担う生理活性物質アンジオテンシンII (Ang II)の受容体であるAT1受容体の生理的な活性化を通じて、交感神経系などとともに、生体の血圧循環調節や腎機能制御を行っており、生体の機能維持に重要な循環調節系です。しかしながら、カロリー過剰摂取や種々のストレスなどの病的な慢性刺激により組織局所でのR-A系のAT1受容体系の過剰活性化が生じることがあり、これが原因となって組織局所での酸化ストレス増加や炎症反応が持続して引き起こされ、生活習慣病とその動脈硬化合併症の発症・進展にも深く関与することが提唱されています。したがって、生活習慣病とその動脈硬化合併症の発症・進展において、Ang II=生活習慣病増悪因子、AT1受容体=生活習慣病増悪因子受容体として捉えることができます。
一方、内蔵脂肪型肥満、インスリン抵抗性を特徴とする生活習慣病とその動脈硬化合併症においては、脂肪組織における脂肪細胞肥大化や脂肪組織での軽度な慢性炎症の病態への関与の可能性、あるいは脂肪組織でのR-A系、AT1受容体系の関与の可能性が指摘されています。しかしながらその分子病態学的な基盤については十分に解明されていませんでした。
*2 インターベンション治療: カテーテルと呼ばれる細いチューブを血管に挿入して行う治療法
*3 集学的治療: 外科的治療・内科的治療・放射線治療など複数の治療法を組み合わせて行う治療法
研究の内容
生活習慣病とその動脈硬化合併症の抑制のためには、組織局所での生活習慣病増悪因子受容体(AT1受容体)の過剰活性化を抑制することが重要と考えられます。これまでに田村准教授は、Harvard大学(現Duke大学)のDzau教授らとともに世界で初めて生活習慣病増悪因子受容体(AT1受容体)への直接結合性機能制御因子として、ATRAP/Agtrapの単離・同定に成功し、その病態生理学的意義の検討と臨床応用への可能性について検討してきました。
本研究では、田村准教授、涌井助教、前田博士ら(GR)が、まず、正常状態においてはATRAPがマウスやヒトの脂肪組織に多く存在していることを初めて明らかにしました。しかしながら、今回生活習慣病のマウスやヒトの脂肪組織においてはATRAPの発現量が減少していることがわかりました。
そこで、発生工学的手法により生まれつきATRAPをもたないATRAP欠損マウスを作成したところ、通常食飼育下では正常マウスと比べて特に変化はみられませんでしたが、肥満を誘発する高脂肪食で飼育した場合には、内臓脂肪型肥満、高血圧、脂質異常症、インスリン抵抗性などの生活習慣病の症状が出現することが明らかになりました。
さらに、ATRAPを高発現している脂肪組織を用いてATRAP欠損マウスの皮下に脂肪組織の移植治療を行うと生活習慣病の症状が改善できることを証明しました。
また、培養細胞を用いてのATRAP遺伝子発現活性化の検討では、マウスやヒトのATRAP遺伝子のプロモーター領域にあるE-boxという転写調節領域に結合するUSF-1、 USF-2という転写調節因子による相互作用が、ATRAP遺伝子の発現活性化に重要であることを明らかにしました。
※本研究は、米学会誌『Journal of American Heart Association(米国心臓病協会誌 AHA Journal)』に掲載されました(米国時間7月31日付オンライン掲載)。“Angiotensin receptor-binding protein ATRAP/Agtrap inhibits metabolic dysfunction with visceral obesity”
本研究では、田村准教授、涌井助教、前田博士ら(GR)が、まず、正常状態においてはATRAPがマウスやヒトの脂肪組織に多く存在していることを初めて明らかにしました。しかしながら、今回生活習慣病のマウスやヒトの脂肪組織においてはATRAPの発現量が減少していることがわかりました。
そこで、発生工学的手法により生まれつきATRAPをもたないATRAP欠損マウスを作成したところ、通常食飼育下では正常マウスと比べて特に変化はみられませんでしたが、肥満を誘発する高脂肪食で飼育した場合には、内臓脂肪型肥満、高血圧、脂質異常症、インスリン抵抗性などの生活習慣病の症状が出現することが明らかになりました。
さらに、ATRAPを高発現している脂肪組織を用いてATRAP欠損マウスの皮下に脂肪組織の移植治療を行うと生活習慣病の症状が改善できることを証明しました。
また、培養細胞を用いてのATRAP遺伝子発現活性化の検討では、マウスやヒトのATRAP遺伝子のプロモーター領域にあるE-boxという転写調節領域に結合するUSF-1、 USF-2という転写調節因子による相互作用が、ATRAP遺伝子の発現活性化に重要であることを明らかにしました。
※本研究は、米学会誌『Journal of American Heart Association(米国心臓病協会誌 AHA Journal)』に掲載されました(米国時間7月31日付オンライン掲載)。“Angiotensin receptor-binding protein ATRAP/Agtrap inhibits metabolic dysfunction with visceral obesity”
今後の展開
本研究成果の意義は、正常時には脂肪組織に多く存在している『生活習慣病増悪因子受容体系の病的な過剰活性化に対する内在性抑制因子』であるATRAPが、生活習慣病の病態においては脂肪組織において減少してしまうことを明らかにした点にあります。
生まれつきATRAPを持たないATRAP欠損マウスでは、通常食では異常がみられないものの、高脂肪食飼育により脂肪細胞の肥大化や脂肪組織の炎症をともないながらインスリン抵抗性や高血圧などの生活習慣病が引き起こされることも証明されました。 さらに、ATRAPが多く存在する脂肪組織を生活習慣病状態のマウスに皮下移植することにより、生活習慣病の病態を改善することに成功したことは、今後脂肪前駆細胞を利用した細胞治療への応用などにより、高リスクの生活習慣病患者や動脈硬化合併症患者に対する新規標的治療の開発に結びつく可能性があります。
本研究で着目したATRAPは、細胞や組織表面に存在する生活習慣病増悪因子受容体(AT1受容体)の細胞内取り込み(internalization)を持続的に促進することにより、正常な生理機能を維持する機能は維持しながら、病的刺激によって生活習慣病増悪因子受容体(AT1受容体)が情報伝達系組織局所で過剰活性化することに対してのみ抑制作用を発揮します。したがって、ATRAPは生活習慣病とその動脈硬化合併症を改善できる可能性をもち、組織バイオマーカー、治療標的として、病態リスク評価や安全で効率的な新規治療開発に大きく貢献すると期待されます。
生まれつきATRAPを持たないATRAP欠損マウスでは、通常食では異常がみられないものの、高脂肪食飼育により脂肪細胞の肥大化や脂肪組織の炎症をともないながらインスリン抵抗性や高血圧などの生活習慣病が引き起こされることも証明されました。 さらに、ATRAPが多く存在する脂肪組織を生活習慣病状態のマウスに皮下移植することにより、生活習慣病の病態を改善することに成功したことは、今後脂肪前駆細胞を利用した細胞治療への応用などにより、高リスクの生活習慣病患者や動脈硬化合併症患者に対する新規標的治療の開発に結びつく可能性があります。
本研究で着目したATRAPは、細胞や組織表面に存在する生活習慣病増悪因子受容体(AT1受容体)の細胞内取り込み(internalization)を持続的に促進することにより、正常な生理機能を維持する機能は維持しながら、病的刺激によって生活習慣病増悪因子受容体(AT1受容体)が情報伝達系組織局所で過剰活性化することに対してのみ抑制作用を発揮します。したがって、ATRAPは生活習慣病とその動脈硬化合併症を改善できる可能性をもち、組織バイオマーカー、治療標的として、病態リスク評価や安全で効率的な新規治療開発に大きく貢献すると期待されます。
お問い合わせ先
(本資料の内容に関するお問い合わせ)
○公立大学法人横浜市立大学 学術院医学群 循環器・腎臓内科学 田村 功一
TEL:045-787-2635 FAX:045-701-3738
E-mail:tamukou@med.yokohama-cu.ac.jp
(取材対応窓口、資料請求など)
○公立大学法人 横浜市立大学 先端医科学研究課長 立石 建
TEL:045-787-2527 FAX:045-787-2509
E-mail:sentan@yokohama-cu.ac.jp
○公立大学法人横浜市立大学 学術院医学群 循環器・腎臓内科学 田村 功一
TEL:045-787-2635 FAX:045-701-3738
E-mail:tamukou@med.yokohama-cu.ac.jp
(取材対応窓口、資料請求など)
○公立大学法人 横浜市立大学 先端医科学研究課長 立石 建
TEL:045-787-2527 FAX:045-787-2509
E-mail:sentan@yokohama-cu.ac.jp