2023.04.11
- TOPICS
- 研究
横浜市立大学大学院医学研究科 循環器・腎臓・高血圧内科学の金井大輔医師、花岡正哲医師、涌井広道准教授、田村功一主任教授、横浜市立大学附属病院 次世代臨床研究センター(Y-NEXT)の土師達也助教、篠田覚助教、感染制御部の加藤英明部長らは、医療法人社団 厚済会の大西俊正博士、三橋洋医師らとの共同研究で、新型コロナウイルスに感染歴のない血液透析患者238名と医療スタッフ58名において、BNT162b2(ファイザー社の従来株型の新型コロナウイルスmRNAワクチン*1)2回目接種1か月後から4回目接種1ヶ月後までの間に測定された抗スパイクタンパク*2抗体の力価を比較検討しました。その結果、血透析患者におけるBNT162b2ワクチンに対する液性免疫反応は、3回目接種までは大幅な上昇反応を示すものの4回目接種では有意に鈍化することを発見・報告しました。
研究成果のポイント
|
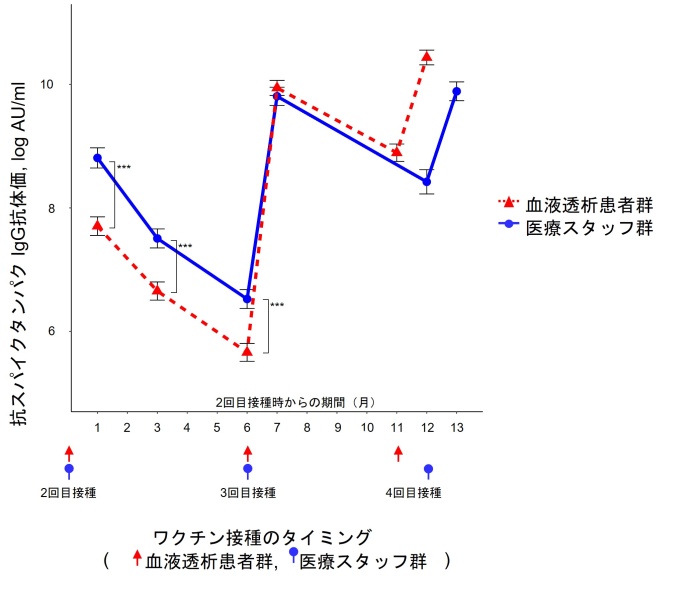 (図1)血液透析患者群と医療スタッフ群毎の抗スパイスタンパク抗体価の上昇幅
(図1)血液透析患者群と医療スタッフ群毎の抗スパイスタンパク抗体価の上昇幅
研究背景
新型コロナウイルスmRNAワクチンはCOVID-19の重症化率を低下させ、死亡率を減少させる効果があると報告されてきました(文献1)。進行した慢性腎臓病をもっている人、特に血液透析を受けている人は、COVID-19の重症化や死亡の危険性が高いことが問題とされ(文献2)、ワクチンを積極的に接種することで、重症化率や死亡率が低下すると報告されました(文献3)。日本国内でも、血液透析を受けている人に対してワクチン接種が強く推奨されてきましたが、進行した慢性腎臓病をもつ人は尿毒素の影響で免疫力が慢性的に低下しており、ワクチンに対する反応が弱いため十分な中和抗体を獲得しにくいとされていました(文献4、5)。
本研究グループは、現在までに、以下の研究結果を世界に先駆けて報告してきました。
① 2回のワクチン接種後に獲得できる抗体価(ピーク値)は、血液透析患者群では健常人(医療スタッフ群)と比べて3分の1程度と有意に低値であり(2617 vs. 7285 AU/ml, p < 0.001,)、ピーク抗体価の上昇に寄与する因子は栄養状態と貧血の改善、ビタミン D の補充である(文献6)。
https://www.yokohama-cu.ac.jp/news/2022/20220628wakuihiromichi.html
② 3回目のワクチン接種によって、血液透析患者群では抗体価が大幅に上昇し、健常人と変わらない程度の抗体価を獲得できる(24,500 AU/mL vs. 20,000AU/mL)(文献8)。従来株の生ウイルスによる細胞死を完全に抑制できる中和抗体価と抗スパイクタンパク抗体価の関係では、抗スパイクタンパク抗体価が997 BAU/mL (= 7021 AU/ml)以上で中和抗体価と正の相関を認めるとされ、血液透析患者においてもワクチンの3回目接種による感染予防効果が期待される(文献8)。
https://www.yokohama-cu.ac.jp/news/2022/20220913wakuihiromichi.html
しかしながら、2022年の年始からオミクロン株の台頭により国内で新規感染者が爆発的に増加(第6波が到来)したため、4回目のワクチン接種を積極的に進める政策が取られました。海外の報告では、4回目の新型コロナmRNAワクチン接種を受けた健康な人の抗体価は3回目接種後と比べて軽度の上昇に留まるとされました(文献9)。しかし、血液透析患者の抗体価に関する報告は症例数が少ない研究に限られており、また東アジア圏内からの報告はありませんでした。そこで、今回、日本人の血液透析患者群と医療スタッフ群を対象に、新型コロナmRNAワクチン(従来株型)4回目接種前後における抗スパイクタンパク抗体価を検討しました。
本研究グループは、現在までに、以下の研究結果を世界に先駆けて報告してきました。
① 2回のワクチン接種後に獲得できる抗体価(ピーク値)は、血液透析患者群では健常人(医療スタッフ群)と比べて3分の1程度と有意に低値であり(2617 vs. 7285 AU/ml, p < 0.001,)、ピーク抗体価の上昇に寄与する因子は栄養状態と貧血の改善、ビタミン D の補充である(文献6)。
https://www.yokohama-cu.ac.jp/news/2022/20220628wakuihiromichi.html
② 3回目のワクチン接種によって、血液透析患者群では抗体価が大幅に上昇し、健常人と変わらない程度の抗体価を獲得できる(24,500 AU/mL vs. 20,000AU/mL)(文献8)。従来株の生ウイルスによる細胞死を完全に抑制できる中和抗体価と抗スパイクタンパク抗体価の関係では、抗スパイクタンパク抗体価が997 BAU/mL (= 7021 AU/ml)以上で中和抗体価と正の相関を認めるとされ、血液透析患者においてもワクチンの3回目接種による感染予防効果が期待される(文献8)。
https://www.yokohama-cu.ac.jp/news/2022/20220913wakuihiromichi.html
しかしながら、2022年の年始からオミクロン株の台頭により国内で新規感染者が爆発的に増加(第6波が到来)したため、4回目のワクチン接種を積極的に進める政策が取られました。海外の報告では、4回目の新型コロナmRNAワクチン接種を受けた健康な人の抗体価は3回目接種後と比べて軽度の上昇に留まるとされました(文献9)。しかし、血液透析患者の抗体価に関する報告は症例数が少ない研究に限られており、また東アジア圏内からの報告はありませんでした。そこで、今回、日本人の血液透析患者群と医療スタッフ群を対象に、新型コロナmRNAワクチン(従来株型)4回目接種前後における抗スパイクタンパク抗体価を検討しました。
研究内容
本研究は、新型コロナウイルスに対するファイザー社製mRNAワクチン(従来株型)の接種を受けた日本人血液透析患者群と医療スタッフ群を対象として、ワクチン接種後に獲得された抗スパイクタンパク抗体の力価の経時的な推移を後方視的に調べたものです。
医療社団法人厚済会では、関連透析施設(上大岡仁正クリニック、文庫じんクリニック、金沢クリニック、追浜仁正クリニック)に通院されている血液透析患者さんと勤務している医療スタッフの中で、2回目のワクチン接種を完了し抗スパイクタンパク抗体検査を希望された方に対して、無料で(抗体検査費用の全額を医療社団法人厚済会が負担)抗体検査が提供されていました。結果は各被検者に通知され、診療録等に記録されていました。3・4回目のワクチン接種後も希望者に対しては継続して検査の機会を設けており、本研究では、保管されていた情報を診療録等から収集し解析を行いました。
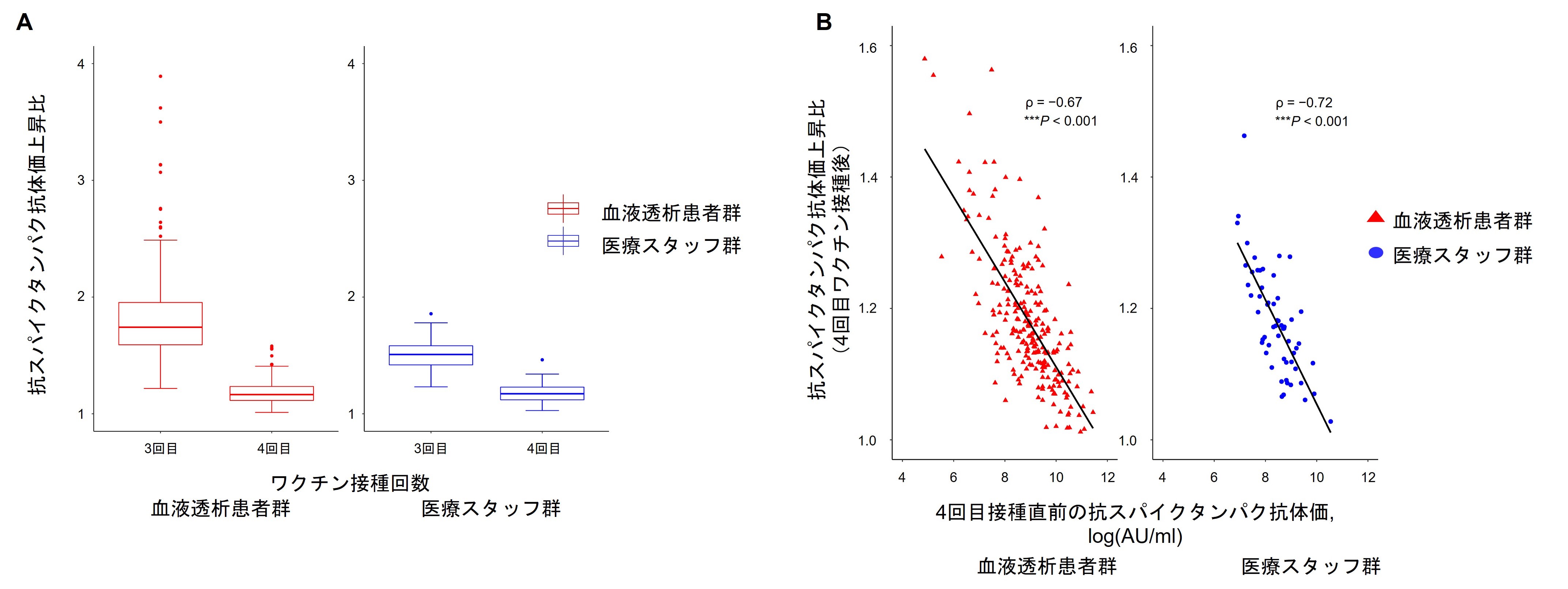
新型コロナウイルス感染歴のない血液透析患者群238名、コントロール群58名のデータを解析しました。4回目のワクチン接種1ヵ月後の抗体価は、3回目接種1ヵ月後のピーク抗体価と比較して、血液透析患者群で約1.5倍の上昇(24,000 → 37,000 AU/ml)、医療スタッフ群ではほぼ等倍(17,500 → 18,500 AU/ml)の変化に留まりました(図2A)。また、背景として4回目のワクチン接種直前の抗体価と接種後の抗体価には負の相関関係(接種前の抗体価が高いとワクチン接種後に抗体価の上昇幅が小さく、接種前の抗体価が低いと、接種後の上昇幅が大きくなること)を認めました(図2B)。これらの結果から、従来株型の新型コロナウイルスmRNAワクチンの場合、接種を繰り返すことでワクチンに対する液性免疫応答が有意に鈍化することが示唆されました。
また、抗体価の減衰速度に関しては、2回目接種1ヵ月後から3回目接種直前までの減衰速度に比べて、3回目接種1ヶ月後から4回目接種直前までの減衰速度は両群共に有意に低下していました(血液透析患者群:-0.409 vs. -0.262 log(AU/ml), p < 0.001,医療スタッフ群:-0.457 vs. -0.277 log(AU/ml), p < 0.001)。つまり、ワクチン接種を繰り返すと、それにより獲得された抗体価は低下しにくくなり、臨床的に有効な抗体力価(血中抗体濃度)を維持するための追加接種の間隔(期間)を延長できる可能性が示されました。(ただし、臨床的に有効とされる抗体力価が一定である場合を想定しています。)
医療社団法人厚済会では、関連透析施設(上大岡仁正クリニック、文庫じんクリニック、金沢クリニック、追浜仁正クリニック)に通院されている血液透析患者さんと勤務している医療スタッフの中で、2回目のワクチン接種を完了し抗スパイクタンパク抗体検査を希望された方に対して、無料で(抗体検査費用の全額を医療社団法人厚済会が負担)抗体検査が提供されていました。結果は各被検者に通知され、診療録等に記録されていました。3・4回目のワクチン接種後も希望者に対しては継続して検査の機会を設けており、本研究では、保管されていた情報を診療録等から収集し解析を行いました。
新型コロナウイルス感染歴のない血液透析患者群238名、コントロール群58名のデータを解析しました。4回目のワクチン接種1ヵ月後の抗体価は、3回目接種1ヵ月後のピーク抗体価と比較して、血液透析患者群で約1.5倍の上昇(24,000 → 37,000 AU/ml)、医療スタッフ群ではほぼ等倍(17,500 → 18,500 AU/ml)の変化に留まりました(図2A)。また、背景として4回目のワクチン接種直前の抗体価と接種後の抗体価には負の相関関係(接種前の抗体価が高いとワクチン接種後に抗体価の上昇幅が小さく、接種前の抗体価が低いと、接種後の上昇幅が大きくなること)を認めました(図2B)。これらの結果から、従来株型の新型コロナウイルスmRNAワクチンの場合、接種を繰り返すことでワクチンに対する液性免疫応答が有意に鈍化することが示唆されました。

ー(図2)抗スパイスタンパク抗体価上昇比較(A:ワクチン接種回数、B:4回目接種直前の抗スパイクタンパク抗体価)
また、抗体価の減衰速度に関しては、2回目接種1ヵ月後から3回目接種直前までの減衰速度に比べて、3回目接種1ヶ月後から4回目接種直前までの減衰速度は両群共に有意に低下していました(血液透析患者群:-0.409 vs. -0.262 log(AU/ml), p < 0.001,医療スタッフ群:-0.457 vs. -0.277 log(AU/ml), p < 0.001)。つまり、ワクチン接種を繰り返すと、それにより獲得された抗体価は低下しにくくなり、臨床的に有効な抗体力価(血中抗体濃度)を維持するための追加接種の間隔(期間)を延長できる可能性が示されました。(ただし、臨床的に有効とされる抗体力価が一定である場合を想定しています。)
今後の展開
血液透析患者は健康な人に比べて、ワクチンに対する免疫反応性が低く獲得できる抗体価が低いと考えられていましたが、新型コロナmRNAワクチンを3回接種することで抗体価が平均で10倍上昇し健常人と同レベルに達することが分かりました。ところが、4回目の接種では抗体価はわずかな上昇に留まり、液性免疫反応の鈍化が明らかになりました。2022年10月(本研究論文執筆時点)ではオミクロン株BA.4/5が蔓延しています。従来株型のmRNAワクチンで得られた抗スパイクタンパク抗体で従来株ウイルスを中和し感染予防効果を得るには7021AU/mL以上の力価が必要とされていますが、BA.4/5株に対してはその11倍以上の抗体価を要するとされています(文献10)。本研究の結果から、従来株型のワクチン接種では、そのような高い抗体価を獲得・維持することは現実的に困難であると分かりました。よって、オミクロン株(BA.4/5)の流行下では、オミクロン株対応ワクチンの接種を進めることが好ましいと考えられました。国内ではオミクロン株対応ワクチンの接種は2022年9月以降に開始されました。血液透析患者を対象としたオミクロン株対応ワクチンの有効性について、国内外からの知見の集積が待たれます。
論文情報
タイトル: Blunted humoral immune response to the fourth dose of BNT162b2 COVID‑19 vaccine in patients undergoing hemodialysis
著者: Daisuke Kanai, Hiromichi Wakui1, Masaaki Hanaoka, Tatsuya Haze, Kengo Azushima, Satoru Shinoda, Shunichiro Tsukamoto, Shinya Taguchi, Sho Kinguchi, Tomohiko Kanaoka, Yoshiyuki Toya, Nobuhito Hirawa, Hideaki Kato, Fumimasa Watanabe, Kanako Hanaoka, Hiroshi Mitsuhashi, Satoshi Yamaguchi, Toshimasa Ohnishi, Kouichi Tamura1
掲載雑誌: Clinical and Experimental Nephrology
DOI: 10.1007/s10157-023-02342-0
著者: Daisuke Kanai, Hiromichi Wakui1, Masaaki Hanaoka, Tatsuya Haze, Kengo Azushima, Satoru Shinoda, Shunichiro Tsukamoto, Shinya Taguchi, Sho Kinguchi, Tomohiko Kanaoka, Yoshiyuki Toya, Nobuhito Hirawa, Hideaki Kato, Fumimasa Watanabe, Kanako Hanaoka, Hiroshi Mitsuhashi, Satoshi Yamaguchi, Toshimasa Ohnishi, Kouichi Tamura1
掲載雑誌: Clinical and Experimental Nephrology
DOI: 10.1007/s10157-023-02342-0
用語解説
*1 mRNAワクチン:
mRNA(メッセンジャーRNA)ワクチンは、ウイルスのタンパク質をつくるもとになる遺伝情報の一部を注射する。人の身体の中で、この情報をもとに、ウイルスのタンパク質の一部が作られ、それに対する抗体が作られる。
*2 抗スパイクタンパク:
新型コロナウイルスの表面にはスパイクタンパク質というものが存在しており、ウイルスが人体の細胞に侵入する際に足掛かりとなる重要なタンパク質である。ウイルス表面のスパイクタンパク質に結合することで、スパイクタンパク質が人体の細胞に足掛かりを作るのを妨害して、ウイルスの体内への侵入を阻害する。ファイザー社やモデルナ社のワクチンの接種によって、抗スパイクタンパク抗体を獲得することができる。
mRNA(メッセンジャーRNA)ワクチンは、ウイルスのタンパク質をつくるもとになる遺伝情報の一部を注射する。人の身体の中で、この情報をもとに、ウイルスのタンパク質の一部が作られ、それに対する抗体が作られる。
*2 抗スパイクタンパク:
新型コロナウイルスの表面にはスパイクタンパク質というものが存在しており、ウイルスが人体の細胞に侵入する際に足掛かりとなる重要なタンパク質である。ウイルス表面のスパイクタンパク質に結合することで、スパイクタンパク質が人体の細胞に足掛かりを作るのを妨害して、ウイルスの体内への侵入を阻害する。ファイザー社やモデルナ社のワクチンの接種によって、抗スパイクタンパク抗体を獲得することができる。
参考文献
(文献1)
Pilishvili T, et al. Effectiveness of mRNA Covid-19 Vaccine among U.S. Health Care Personnel. N Engl J Med 2021; 385(25): e90.
(文献2)
Kikuchi K, et al. Survival and predictive factors in dialysis patients with COVID-19 in Japan: a nationwide cohort study. Ren Replace Ther 2021;7(1):59.
(文献3)
Chung EYM, et al. Incidence and Outcomes of COVID-19 in People With CKD: A Systematic Review and Meta-analysis. Am J Kidney Dis 2021; 78(6): 804-15.
(文献4)
Sibbel S, et al. Real-World Effectiveness and Immunogenicity of BNT162b2 and mRNA-1273 SARS-CoV-2 Vaccines in Patients on Hemodialysis. J Am Soc Nephrol 2022; 33(1): 49-57.
(文献5)
Ghadiani MH, et al. Response rates to HB vaccine in CKD stages 3-4 and hemodialysis patients. J Res Med Sci 2012; 17(6): 527-33.
(文献6)
Kanai D, et al. SARS-CoV-2 spike protein antibody titers 6 months after SARS-CoV-2 mRNA vaccination among patients undergoing hemodialysis in Japan. Clin Exp Nephrol. 2022. doi: 10.1007/s10157-022-02243-8.
(文献7)
Kanai D, et al. Improved immune response to the third COVID-19 mRNA vaccine dose in hemodialysis patient. Kidney Int Rep. 2022 Dec;7(12):2718-2721. doi: 10.1016/j.ekir.2022.09.005.
(文献8)
Espi M, et al. A prospective observational study for justification, safety, and efficacy of a third dose of mRNA vaccine in patients receiving maintenance hemodialysis. Kidney Int 2022; 101(2): 390-402.
(文献9)
Syversen SW, et al. Immunogenicity and safety of standard and third-dose SARS-CoV-2 vaccination in patients receiving immunosuppressive therapy. Arthritis Rheumatol. 2022. doi: 10.1002/art.42153.
(文献10)
Tuekprakhon A, et al. Antibody escape of SARS-CoV-2 Omicron BA.4 and BA.5 from vaccine and BA.1 serum. Cell 2022; 185(14): 2422-33.e13.
Pilishvili T, et al. Effectiveness of mRNA Covid-19 Vaccine among U.S. Health Care Personnel. N Engl J Med 2021; 385(25): e90.
(文献2)
Kikuchi K, et al. Survival and predictive factors in dialysis patients with COVID-19 in Japan: a nationwide cohort study. Ren Replace Ther 2021;7(1):59.
(文献3)
Chung EYM, et al. Incidence and Outcomes of COVID-19 in People With CKD: A Systematic Review and Meta-analysis. Am J Kidney Dis 2021; 78(6): 804-15.
(文献4)
Sibbel S, et al. Real-World Effectiveness and Immunogenicity of BNT162b2 and mRNA-1273 SARS-CoV-2 Vaccines in Patients on Hemodialysis. J Am Soc Nephrol 2022; 33(1): 49-57.
(文献5)
Ghadiani MH, et al. Response rates to HB vaccine in CKD stages 3-4 and hemodialysis patients. J Res Med Sci 2012; 17(6): 527-33.
(文献6)
Kanai D, et al. SARS-CoV-2 spike protein antibody titers 6 months after SARS-CoV-2 mRNA vaccination among patients undergoing hemodialysis in Japan. Clin Exp Nephrol. 2022. doi: 10.1007/s10157-022-02243-8.
(文献7)
Kanai D, et al. Improved immune response to the third COVID-19 mRNA vaccine dose in hemodialysis patient. Kidney Int Rep. 2022 Dec;7(12):2718-2721. doi: 10.1016/j.ekir.2022.09.005.
(文献8)
Espi M, et al. A prospective observational study for justification, safety, and efficacy of a third dose of mRNA vaccine in patients receiving maintenance hemodialysis. Kidney Int 2022; 101(2): 390-402.
(文献9)
Syversen SW, et al. Immunogenicity and safety of standard and third-dose SARS-CoV-2 vaccination in patients receiving immunosuppressive therapy. Arthritis Rheumatol. 2022. doi: 10.1002/art.42153.
(文献10)
Tuekprakhon A, et al. Antibody escape of SARS-CoV-2 Omicron BA.4 and BA.5 from vaccine and BA.1 serum. Cell 2022; 185(14): 2422-33.e13.

