新しい血圧コントロールの仕組みを解明
2017.09.25
- TOPICS
- 研究
- 医療
新しい血圧コントロールの仕組みを解明
JCI Insightに掲載
横浜市立大学 学術院医学群 薬理学 五嶋良郎教授らの研究グループは、同循環器・腎臓・高血圧内科学、循環制御医学教室と共同で、血圧が昼夜で変動する新たな仕組みを明らかにしました。血圧は、心臓と血管の働きを通じ、交感神経や副交感神経と呼ばれる自律神経系によってコントロールされることが知られています。我々は、主に交感神経から遊離されるノルアドレナリン*1という血管収縮物質に対する血管の反応性が、ノルアドレナリンの原料となるドーパというアミノ酸によってコントロールされていることを明らかにしました。ドーパ*2の作用がなくなると、マウスは昼と夜の適切な血圧のコントロールができず、いわゆる「朝に弱い」(マウスは夜行性なので、実際には「夜に弱い」)状態に陥ることが明らかになりました。
本成果は、従来の治療法では血圧のコントロールが困難な高血圧症や、それに伴う心疾患、腎疾患の新しい治療法につながることが期待されます。
本成果は、従来の治療法では血圧のコントロールが困難な高血圧症や、それに伴う心疾患、腎疾患の新しい治療法につながることが期待されます。
| 研究成果のポイント ○ドーパによるこれまでとは異なる血圧コントロールの仕組みが判明した。 ○従来の治療法が効かなかった高血圧症を異なるアプローチで改善することが期待される。 |
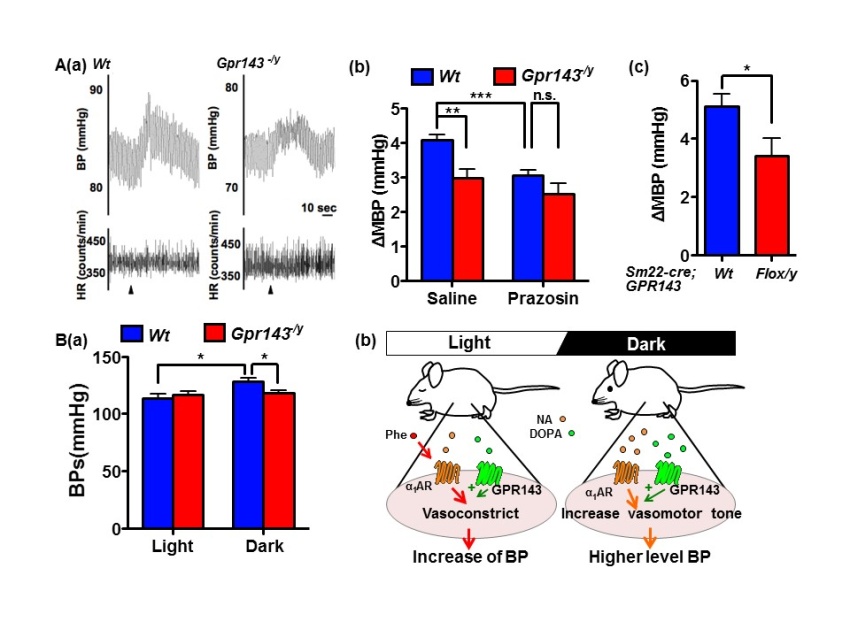 (図)A:GPR143-KOマウスでは、刺激による血圧の上昇が低下する。 B:GPR143-KOマウスでは夜間の血圧上昇が起こらなくなる。
(図)A:GPR143-KOマウスでは、刺激による血圧の上昇が低下する。 B:GPR143-KOマウスでは夜間の血圧上昇が起こらなくなる。
研究の背景と経緯
高血圧症とこれに伴う血圧変動幅の大きさは、心筋梗塞、不整脈などの心疾患、糖尿病や腎不全などのリスクファクターであり、これらは血圧の不適切な管理によって起こる生活習慣病と言われています。血圧制御異常に対する治療は、食事や運動療法に加え、抗高血圧薬が重要な位置づけを占めており、抗高血圧薬は、利尿薬、カルシウム拮抗薬、アンジオテンシン阻害薬などがあります。病態に応じて様々な治療が行われていますが、依然として難治の高血圧症が存在します。
ドーパは、神経伝達物質ドパミンの前駆体として位置づけられていますが、五嶋教授らは、ドーパがそれ自体で神経伝達物質ないし修飾物質として働くことを世界に先駆けて示してきました(Misu and Goshima, TiPS 14; 119-123, 1993)。また最近、ドーパ受容体としてGPR143を同定し、この受容体が、脳幹部孤束核において、降圧薬や除脈性応答を仲介することを示しました(Hiroshima et al., Br J Pharmacol 171 403-414, 2014)。このドーパ受容体GPR143の遺伝子欠損(GPR143-KO)マウスを解析したところ、フェニレフリンというα1—アドレナリン受容体作動薬を静脈内注射した際の昇圧応答が、GPR143-KOマウスでは減弱していることを発見し、これが本研究着想のきっかけとなりました。
ドーパは、神経伝達物質ドパミンの前駆体として位置づけられていますが、五嶋教授らは、ドーパがそれ自体で神経伝達物質ないし修飾物質として働くことを世界に先駆けて示してきました(Misu and Goshima, TiPS 14; 119-123, 1993)。また最近、ドーパ受容体としてGPR143を同定し、この受容体が、脳幹部孤束核において、降圧薬や除脈性応答を仲介することを示しました(Hiroshima et al., Br J Pharmacol 171 403-414, 2014)。このドーパ受容体GPR143の遺伝子欠損(GPR143-KO)マウスを解析したところ、フェニレフリンというα1—アドレナリン受容体作動薬を静脈内注射した際の昇圧応答が、GPR143-KOマウスでは減弱していることを発見し、これが本研究着想のきっかけとなりました。
研究の内容
我々は、心血管機能における GPR143 の役割を解明するため、フェニレフリンによる昇圧応答を GPR143-KOマウスを用いて検討し、その結果、GPR143-KOマウスにおいてフェニレフリンによる昇圧応答が著減していることを発見しました。さらに、血管平滑筋特異的に GPR143 を欠損させた動物においてもフェニレフリン応答の著減が認められました。
野生型とGPR143-KOマウスからの摘出血管標本を用いて比較・検討したところ、GPR143-KO マウスの血管ではフェニレフリンによる血管収縮作用が減弱していました。また、摘出血管において、ドーパ(10 nM)はフェニレフリンによる血管収縮応答を増強する一方、GPR143-KO血管においてはドーパによる増強作用は認められませんでした。
活動・睡眠時の血中ドーパ濃度は、活動期の夜間で高く(10 nM)睡眠期で低値(5 nM)を示し、さらに、無麻酔無拘束下の24 時間血圧・心拍数の変動をテレメトリー法により測定したところ、野生型で認められる夜間の血圧上昇・心拍数の増大は、GPR143-KO マウスでは野生型に比べ減弱していました。これらの知見は、GPR143 が、血管における交感神経応答の制御を介して、血圧の日内変動に関与することを示します。FRETという方法で解析したところ、GPR143はα1—アドレナリン受容体と直接相互作用して、交感神経の伝達物質であるノルアドレナリンに対する感受性を高めていることも明らかとなりました。
野生型とGPR143-KOマウスからの摘出血管標本を用いて比較・検討したところ、GPR143-KO マウスの血管ではフェニレフリンによる血管収縮作用が減弱していました。また、摘出血管において、ドーパ(10 nM)はフェニレフリンによる血管収縮応答を増強する一方、GPR143-KO血管においてはドーパによる増強作用は認められませんでした。
活動・睡眠時の血中ドーパ濃度は、活動期の夜間で高く(10 nM)睡眠期で低値(5 nM)を示し、さらに、無麻酔無拘束下の24 時間血圧・心拍数の変動をテレメトリー法により測定したところ、野生型で認められる夜間の血圧上昇・心拍数の増大は、GPR143-KO マウスでは野生型に比べ減弱していました。これらの知見は、GPR143 が、血管における交感神経応答の制御を介して、血圧の日内変動に関与することを示します。FRETという方法で解析したところ、GPR143はα1—アドレナリン受容体と直接相互作用して、交感神経の伝達物質であるノルアドレナリンに対する感受性を高めていることも明らかとなりました。
今後の展開
今回の成果には、大きく分けて二つの意義があります。一つは、ドーパが神経修飾物質として作動すること、もう一つは、ドーパとドーパ受容体GPR143が、交感神経系を介して血圧をコントロールする全く新しい血圧調節のメカニズムを明らかにした点です。現在、ドーパ及びドーパ受容体を標的にした治療薬は皆無であり、今後、本知見を踏まえた新しい創薬と治療法の確立が期待されます。
用語説明
*1 ノルアドレナリン
交感神経節後線維における神経伝達物質として作用する。ノルアドレナリンは交感神経や副腎髄質細胞から分泌され、心臓、血管に作用して心拍数や血管を収縮させ、血圧を上昇させる。また脂肪細胞である褐色細胞に作用し、熱産生を促す。
*2 ドーパ
レボドパとも言う。パーキンソン病の特効薬である。準必須アミノ酸であるチロシンからチロシン水酸化酵素により交感神経や脳内で合成される。ドーパは生体内に入ると脱炭酸酵素によりドパミンとなる。すなわち、ドーパは、総称的にカテコールアミンとして知られる神経伝達物質である、ドパミン、ノルアドレナリン、アドレナリンの前駆体である。従来は、ドーパはあくまで前駆体であり、それ自体には生理活性がないと信じられてきた。
交感神経節後線維における神経伝達物質として作用する。ノルアドレナリンは交感神経や副腎髄質細胞から分泌され、心臓、血管に作用して心拍数や血管を収縮させ、血圧を上昇させる。また脂肪細胞である褐色細胞に作用し、熱産生を促す。
*2 ドーパ
レボドパとも言う。パーキンソン病の特効薬である。準必須アミノ酸であるチロシンからチロシン水酸化酵素により交感神経や脳内で合成される。ドーパは生体内に入ると脱炭酸酵素によりドパミンとなる。すなわち、ドーパは、総称的にカテコールアミンとして知られる神経伝達物質である、ドパミン、ノルアドレナリン、アドレナリンの前駆体である。従来は、ドーパはあくまで前駆体であり、それ自体には生理活性がないと信じられてきた。
掲載論文
L-DOPA sensitizes vasomotor tone by modulating the vascular alpha1-adrenergic receptor
Daiki Masukawa, Motokazu Koga, Anna Sezaki, Yuka Nakao, Yuji Kamikubo,
Tatsuo Hashimoto, Yuki Okuyama-Oki, Aderemi Caleb Aladeokin, Fumio Nakamura,
Utako Yokoyama, Hiromichi Wakui, Hiroshi Ichinose, Takashi Sakurai, Satoshi Umemura,
Koichi Tamura, Yoshihiro Ishikawa, and Yoshio Goshima
JCI Insight. 2017;2(18):e90903. https://doi.org/10.1172/jci.insight.90903.
※本研究は、米国科学誌『JCI Insight』に掲載されました。(米国東部時間9月21日午前9時付:日本時間9月22日午後10時付オンライン)
※本研究は、科学研究費補助金(基盤B)、及び文部科学省イノベーションシステム整備事業 先端融合領域イノベーション創出拠点形成プログラム「翻訳後修飾プロテオミクス医療研究拠点の形成」の支援を受けて行われました。
Daiki Masukawa, Motokazu Koga, Anna Sezaki, Yuka Nakao, Yuji Kamikubo,
Tatsuo Hashimoto, Yuki Okuyama-Oki, Aderemi Caleb Aladeokin, Fumio Nakamura,
Utako Yokoyama, Hiromichi Wakui, Hiroshi Ichinose, Takashi Sakurai, Satoshi Umemura,
Koichi Tamura, Yoshihiro Ishikawa, and Yoshio Goshima
JCI Insight. 2017;2(18):e90903. https://doi.org/10.1172/jci.insight.90903.
※本研究は、米国科学誌『JCI Insight』に掲載されました。(米国東部時間9月21日午前9時付:日本時間9月22日午後10時付オンライン)
※本研究は、科学研究費補助金(基盤B)、及び文部科学省イノベーションシステム整備事業 先端融合領域イノベーション創出拠点形成プログラム「翻訳後修飾プロテオミクス医療研究拠点の形成」の支援を受けて行われました。
お問い合わせ先
(本資料の内容に関するお問い合わせ)
学術院 医学群薬理学教授五嶋 良郎
TEL:045-787-2593
E-mail:goshima@yokohama-cu.ac.jp
(取材対応窓口、資料請求など)
横浜市立大学研究企画・産学連携推進課長渡邊誠
Tel:045-787-2510
E-mail:
学術院 医学群薬理学教授五嶋 良郎
TEL:045-787-2593
E-mail:goshima@yokohama-cu.ac.jp
(取材対応窓口、資料請求など)
横浜市立大学研究企画・産学連携推進課長渡邊誠
Tel:045-787-2510
E-mail: