ヒト細胞の染色体に外来遺伝子が組み込まれるメカニズムを解明
2017.07.12
- TOPICS
- 研究
ヒト細胞の染色体に外来遺伝子が組み込まれるメカニズムを解明
『Nature Communications』に掲載
横浜市立大学 大学院生命ナノシステム科学研究科の足立典隆 教授と斎藤慎太 博士研究員は、細胞外から導入したDNA(外来遺伝子)が染色体に組み込まれる反応に必要な因子を特定することに成功しました。この発見により、30年以上も不明であった基本的な生命現象の分子メカニズムの一端が明らかになり、外来遺伝子を染色体の狙った位置にだけ組み込むことが可能になりました。 安全なゲノム編集技術への応用が期待されます。
| 成果のポイント ・ DNA 合成酵素PolQ とDNA 連結酵素Lig4 を共に失ったヒト細胞(「hQ4 細胞」と命名)は、外来遺伝子を染色体中に取り込むことができない。 ・「hQ4 細胞」では、遺伝子ターゲティング(染色体の狙った位置にだけ外来遺伝子を取り込ませる安全なゲノム改変技術)を効率100%で行うことができる。 |
研究の背景
外来遺伝子を細胞の中に導入すると、ごく稀に染色体中のランダムな位置に取り込まれます(およそ1,000個の細胞に1個の割合)。この現象は、タンパク質の機能解析をはじめ、有用タンパク質の大量産生、遺伝子組換え作物やiPS 細胞の作製など、さまざまな分野に利用されてきました。しかし、こうしたランダムな組込みによって重要な遺伝子が壊れたり働いてはいけない遺伝子が働いたりする恐れがあるため、本来であれば染色体中の狙った位置に外来遺伝子を組み込ませるほうが安全かつ好都合です。ところが、このような「狙い撃ちの組込み(これを遺伝子ターゲティング※1 と呼びます)」はランダムな組込みの1,000分の1以下の頻度でしか起こらないため、高い効率で遺伝子ターゲティングを行うためにはランダムな組込みをほぼ完全に抑制しなければなりません。この戦略の実現に向けさまざまな研究が行われてきましたが、ヒト細胞での大きな成功例はありませんでした。ランダムな組込みは一見とても単純な生命現象ですが、実際の反応は複雑な再編成を伴うことが多く、その分子メカニズムは30年以上も不明のままでした。
外来遺伝子の組込みは染色体が切れている場所で起こりやすいと考えられています。染色体の切断(二本鎖DNA 切断)は再連結されないと細胞死や癌化を招いてしまうため、相同組換え※2 や非相同末端連結(NHEJ)※3、によって速やかに修復されます。「狙い撃ちの組込み」には相同組換えの働きが必要不可欠です。一方、ランダムな組込みにはNHEJ が関与していますが、NHEJ を欠損させた細胞でもランダムな組込みはほぼ正常に起こります。このため、オルタナティブ末端連結(A-EJ)※4 と呼ばれる別の修復機構の関与が示唆されていましたが、その詳細はよくわかっていませんでした。
外来遺伝子の組込みは染色体が切れている場所で起こりやすいと考えられています。染色体の切断(二本鎖DNA 切断)は再連結されないと細胞死や癌化を招いてしまうため、相同組換え※2 や非相同末端連結(NHEJ)※3、によって速やかに修復されます。「狙い撃ちの組込み」には相同組換えの働きが必要不可欠です。一方、ランダムな組込みにはNHEJ が関与していますが、NHEJ を欠損させた細胞でもランダムな組込みはほぼ正常に起こります。このため、オルタナティブ末端連結(A-EJ)※4 と呼ばれる別の修復機構の関与が示唆されていましたが、その詳細はよくわかっていませんでした。
研究の内容
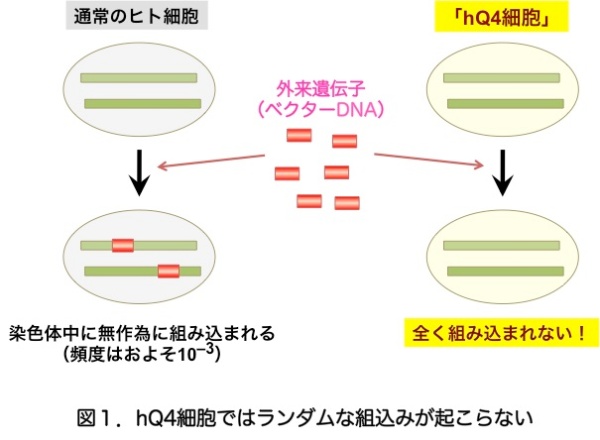
足立教授らはまず、NHEJ に必須なDNA 連結酵素「Lig4(リガーゼ4)」を欠損したヒト細胞におけるランダムな組込みの特徴を網羅的に解析しました。すると、DNA 合成酵素の一つ「PolQ(ポリメラーゼθ)」の関与を示唆するDNA配列上の特徴が連結部位に頻繁に見られました。そこで、PolQとLig4を共に欠損した遺伝子改変細胞※5(「hQ4 細胞」と命名)を構築し、解析を進めたところ、「hQ4 細胞」では導入した外来遺伝子(ベクター)が染色体中に全く組み込まれないことがわかりました(図1)。PolQ のみを欠損した細胞ではランダムな組込みはほぼ正常に起こっていました。
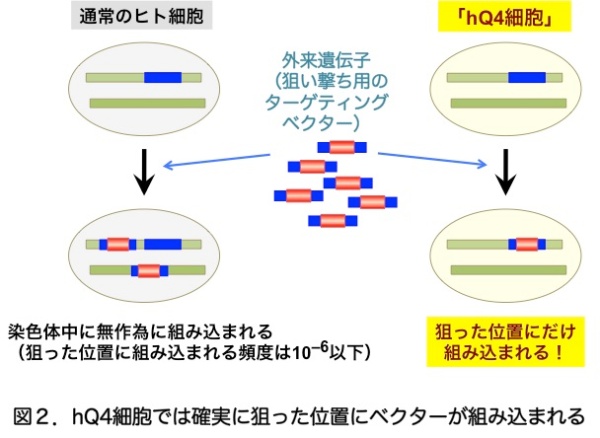
ランダムな組込みが起こらないということは、「狙い撃ちの組込み」のためのベクター(ターゲティングベクター)を用いて実験を行った場合、ベクターの組込みが起こるとすればそれは染色体中の狙った位置でしか起こらないはずです。このことを実験的に検証したところ、予想通り「hQ4 細胞」ではランダムな組込みが全く観察されませんでしたが、狙い撃ちの組込みは低頻度ながら正常に起こっていました。つまり、「hQ4 細胞」では、ランダムな組込みが起こらない一方で相同組換えは正常に機能しているため、100%という高い効率で遺伝子ターゲティングを行えることがわかったのです(図2)。
NHEJ を介した組込みとPolQ を介した組込みのメカニズムの違いを明らかにするため、実際に染色体に組み込まれたベクターの近傍の配列を詳しく解析したところ、前者ではベクターDNA と染色体DNA がほぼそのまま連結されていたのに対し、後者のPolQ を介した反応では複雑な再編成を伴うケースや連結部分に痕跡(特徴的な配列)が残されるケースが多いことがわかりました。ランダムな組込みが「単純な生命現象なのに実際には複雑」であることの理由はPolQ というユニークな酵素の働きに起因していたのです。
さらに足立教授らは、NHEJ が正常に機能している細胞でPolQ を欠損させても二本鎖DNA 切断の修復効率に大きな影響が見られないのに対し、「hQ4 細胞」では染色体DNAが切断された際の修復効率が著しく低下しており、ごく稀に起こる反復DNA 間での組換えでしか切断DNAの再連結が起こらないことを発見しました。ヒトゲノムの約半数は反復DNA(短い繰返し配列)で占められているため、こうした組換えはがん化や遺伝病の原因となるゲノム変化を引き起こしてしまいます。こうした危険な反応がPolQ の働きによって抑えられていることが今回の研究から明らかになりました。
さらに足立教授らは、NHEJ が正常に機能している細胞でPolQ を欠損させても二本鎖DNA 切断の修復効率に大きな影響が見られないのに対し、「hQ4 細胞」では染色体DNAが切断された際の修復効率が著しく低下しており、ごく稀に起こる反復DNA 間での組換えでしか切断DNAの再連結が起こらないことを発見しました。ヒトゲノムの約半数は反復DNA(短い繰返し配列)で占められているため、こうした組換えはがん化や遺伝病の原因となるゲノム変化を引き起こしてしまいます。こうした危険な反応がPolQ の働きによって抑えられていることが今回の研究から明らかになりました。
今後の展開
本研究により、30 年以上も不明であった外来遺伝子のランダムな組込みのメカニズムの一端が明らかになりました。昨今脚光を浴びているCRISPR/Cas9 に代表される人工ヌクレアーゼによるゲノム編集では、オフターゲット変異の発生や不完全なタンパク質の発現が予測不可能であることなど、安全面や技術面においてさまざまな課題が残されています。NHEJ とPolQ を同時に抑制すれば遺伝子ターゲティングを効率100%で行えるという今回の驚くべき発見は、ゲノム編集における一つのブレイクスルーになると考えられ、人工ヌクレアーゼに依らない安全なゲノム改変技術の開発に弾みがつくことが期待されます。
一方、今回の研究結果から、マイナーな修復機構であるA-EJ にPolQ が必要不可欠であることが証明されました。興味深いことに、PolQ は乳癌や卵巣癌をはじめとするさまざまな種類の癌で高発現していることが知られており、しかも悪性度や予後と深い相関があることがわかっています。PolQ 阻害剤はこういった癌の治療に有効であると考えられており、現在世界中で開発が進められています。今回のPolQ に関する新知見から、こうした阻害剤の開発研究にも拍車がかかることが予想されます。
一方、今回の研究結果から、マイナーな修復機構であるA-EJ にPolQ が必要不可欠であることが証明されました。興味深いことに、PolQ は乳癌や卵巣癌をはじめとするさまざまな種類の癌で高発現していることが知られており、しかも悪性度や予後と深い相関があることがわかっています。PolQ 阻害剤はこういった癌の治療に有効であると考えられており、現在世界中で開発が進められています。今回のPolQ に関する新知見から、こうした阻害剤の開発研究にも拍車がかかることが予想されます。
<用語説明>
※1遺伝子ターゲティング:標的遺伝子破壊とも呼ばれる。細胞の核の中で起こる相同組換え反応を利用して、ゲノム上の特定の遺伝子を改変(破壊または修正)する手法のこと。これまで、マウスES細胞を用いた遺伝子ターゲティングにより、世界中で多種多様なノックアウトマウスが作製されてきた。目的の遺伝子以外には傷をつけない理想的な遺伝子治療法として期待されているが、マウスES細胞以外の細胞では効率が極めて低いため、ブレイクスルーが求められていた。
※2相同組換え:DNA の相同性を利用して起こる正確な組換え。生殖細胞の多様性を生み出すのに必須の機構である。一般に、体細胞における相同組換えは姉妹染色分体を利用するため、細胞周期のS/G2 期でしか起こらない。
※3NHEJ(エヌ・エイチ・イー・ジェイ):非相同末端連結(英語表記したときの頭文字を並べるとNHEJ)。DNA の相同性とは無関係に起こる組換えであり、切断されたDNA 末端を効率良く連結できる。しかし、再連結後に短い塩基の挿入や欠失などの変異が導入されてしまうため、効率は良いが不正確な修復である。Ku70、Ku80、Xrcc4、Lig4(DNA リガーゼ4)など複数のタンパク質が関与している。抗体やT 細胞受容体の多様性を生み出すために必須の機構であり、この機構を欠損すると免疫不全となる。また、NHEJ の欠損は小頭症や小人症の原因にもなっている。
※4A-EJ:オルタナティブ末端連結。DNA の相同性とは無関係に起こる、NHEJ 以外の末端連結反応の総称。NHEJ よりもさらに修復の正確度が低い。メカニズムの詳細は長年の間不明であったが、今回の研究から、PolQ(DNA ポリメラーゼθ(シータ))の関与が必須であることが明らかになった。
※5遺伝子改変細胞:遺伝子ターゲティング等の手法によって、特定の遺伝子を人為的に改変した細胞。最近ではCRISPR/Cas9 に代表される人工ヌクレアーゼによるゲノム改変が盛んに行われているが、安全面での課題が残されている。
※2相同組換え:DNA の相同性を利用して起こる正確な組換え。生殖細胞の多様性を生み出すのに必須の機構である。一般に、体細胞における相同組換えは姉妹染色分体を利用するため、細胞周期のS/G2 期でしか起こらない。
※3NHEJ(エヌ・エイチ・イー・ジェイ):非相同末端連結(英語表記したときの頭文字を並べるとNHEJ)。DNA の相同性とは無関係に起こる組換えであり、切断されたDNA 末端を効率良く連結できる。しかし、再連結後に短い塩基の挿入や欠失などの変異が導入されてしまうため、効率は良いが不正確な修復である。Ku70、Ku80、Xrcc4、Lig4(DNA リガーゼ4)など複数のタンパク質が関与している。抗体やT 細胞受容体の多様性を生み出すために必須の機構であり、この機構を欠損すると免疫不全となる。また、NHEJ の欠損は小頭症や小人症の原因にもなっている。
※4A-EJ:オルタナティブ末端連結。DNA の相同性とは無関係に起こる、NHEJ 以外の末端連結反応の総称。NHEJ よりもさらに修復の正確度が低い。メカニズムの詳細は長年の間不明であったが、今回の研究から、PolQ(DNA ポリメラーゼθ(シータ))の関与が必須であることが明らかになった。
※5遺伝子改変細胞:遺伝子ターゲティング等の手法によって、特定の遺伝子を人為的に改変した細胞。最近ではCRISPR/Cas9 に代表される人工ヌクレアーゼによるゲノム改変が盛んに行われているが、安全面での課題が残されている。
掲載論文
Dual loss of human POLQ and LIG4 abolishes random integration.
Shinta Saito, Ryo Maeda & Noritaka Adachi
Nature Communications 8, 16112 doi: 10.1038/ncomms16112 (2017)
※ 本研究は、文部科学省科学研究費補助金、横浜市立大学戦略的研究推進事業(学長裁量事業)などの助成により行われました。また、横浜市立大学先端医科学研究センターが推進している「研究開発プロジェクト」の成果のひとつです。
Shinta Saito, Ryo Maeda & Noritaka Adachi
Nature Communications 8, 16112 doi: 10.1038/ncomms16112 (2017)
※ 本研究は、文部科学省科学研究費補助金、横浜市立大学戦略的研究推進事業(学長裁量事業)などの助成により行われました。また、横浜市立大学先端医科学研究センターが推進している「研究開発プロジェクト」の成果のひとつです。